新加坡国立大学(NUS)研究人员开发出一项生化技术,可捕捉新合成蛋白质与细胞内辅助因子之间短暂的相互作用。研究团队表示,这类“短暂握手”对蛋白质命运至关重要,决定其能否正确折叠并发挥功能,或因缺陷而被细胞清除。相关研究已发表于《分子细胞》(Molecular Cell)。
细胞需要持续合成大量蛋白质以维持生命活动。研究人员指出,蛋白质的生成不仅是按序连接氨基酸链,在合成过程中,新生蛋白链还必须同步折叠成正确的三维结构,并避免与不恰当的分子发生错误结合。
当折叠过程出现偏差时,错误折叠蛋白可能变得更易黏附并发生聚集,从而损害细胞健康。为降低风险,细胞会在蛋白质仍处于合成阶段时进行质量监控。不过,由于参与早期监控的分子与新生蛋白链的接触往往极为短暂,相关关键因子的识别长期面临技术难题。
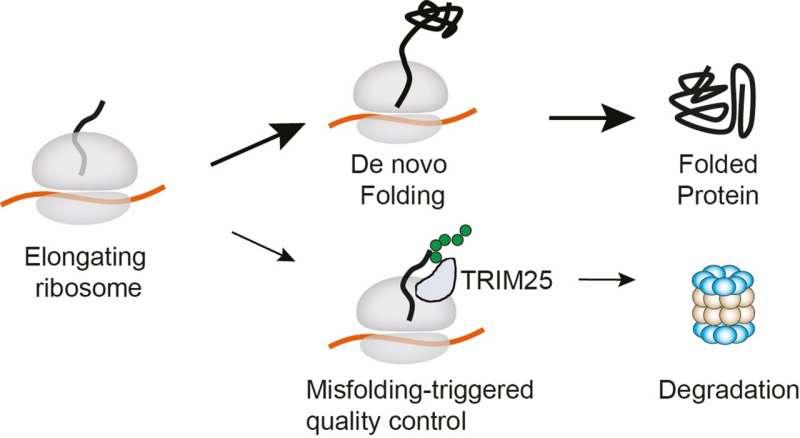
NCIP方法用于固定并识别短暂相互作用
为解决上述问题,由NUS生物科学系助理教授林哲旺(LIN Zhewang)领导的团队提出“新生链相互作用蛋白谱分析”(Nascent Chain Interactor Profiling,NCIP)方法,旨在将这些短暂相互作用“延长”到可被研究的时间尺度。
研究团队介绍,NCIP结合了对新合成蛋白的代谢标记与细胞内化学交联技术,通过将相邻分子固定在一起,研究人员得以富集并鉴定与核糖体上新生蛋白链发生短暂接触的蛋白伙伴,从而为系统性描绘蛋白质合成过程中的分子互作网络提供工具。
借助NCIP,团队鉴定出一种关键酶TRIM25。研究结果显示,TRIM25能够识别从核糖体“出现”的错误折叠蛋白,并在其积累造成损害前对其进行标记,引导进入细胞清除系统。其机制之一是为缺陷蛋白附加名为“泛素”的小分子标签。
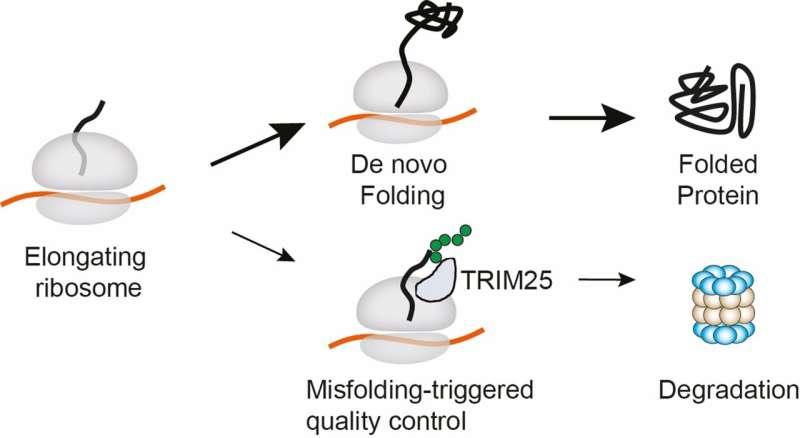
研究指向神经退行性疾病与癌症相关议题
研究人员指出,错误折叠与聚集蛋白的积累是多种神经退行性疾病的特征之一。研究结果表明,TRIM25在共翻译质量控制通路中发挥作用,帮助清除缺陷新生蛋白、抑制其积累;据此,团队认为TRIM25依赖的监控功能受损可能与疾病易感性或疾病进展相关。
研究还提及潜在的肿瘤相关性。快速增殖的肿瘤细胞通常需要合成大量蛋白质,并可能承受较高水平的蛋白毒性应激。在这一背景下,更强的蛋白质质量控制可能有利于癌细胞生存与生长,使TRIM25及相关通路成为后续研究关注方向。
林哲旺表示,蛋白质命运的多项关键决定发生在其合成过程中;通过NCIP,研究人员能够系统捕捉这些短暂相互作用,并识别如TRIM25等因子,从而帮助细胞更早检测并清除错误折叠蛋白,避免问题扩大。











