为确保有性生殖产生健康后代,卵母细胞在细胞分裂后需要获得正确数量的DNA。但随着母体年龄增长,染色体分离更容易出现差错。理化学研究所(RIKEN)研究人员报告称,他们提出并验证了一种基于“人工动粒”的策略,可能有助于减少此类错误并改善卵母细胞生成质量。
卵母细胞通过减数分裂形成。在这一过程中,每条染色体先复制形成X形结构,两条复制体在着丝粒处相连,并由黏连素等蛋白复合体将其锁定在一起。随后,来自分裂细胞两极的微管纤维与染色体上的动粒结构结合,最终将两条染色体复制体拉向相反方向,使新形成的细胞各获得一份染色体拷贝。
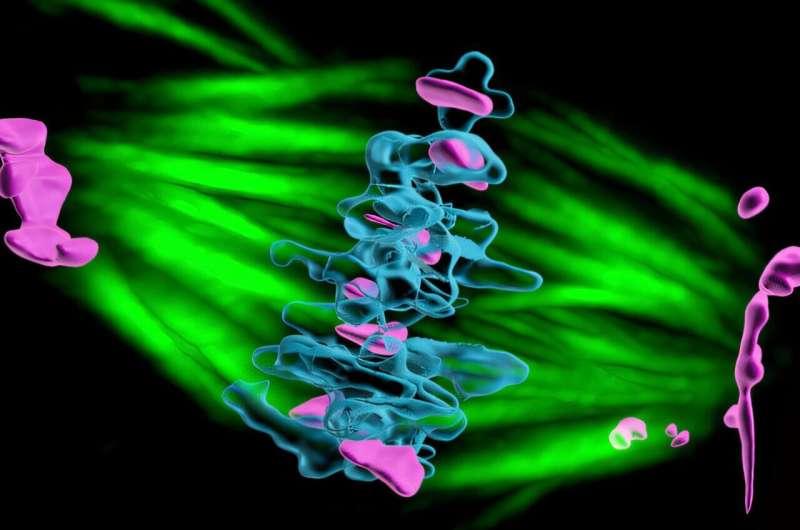
研究团队指出,衰老会削弱卵母细胞染色体的黏连性。理研生物系统动力学研究中心的北岛智也(Tomoya Kitajima)表示,基于小鼠模型的研究显示,卵母细胞染色体上的黏连素复合体数量会随年龄逐渐减少;类似现象很可能也存在于衰老的人类卵母细胞中。在黏连性下降的情况下,原本应保持连接的染色体可能过早分离,导致基因组物质分配异常,进而使卵子出现发育缺陷或无法产生可存活后代。
北岛团队最初的研究目标是构建一种人工动粒——即减数分裂中微管附着的染色体结构。团队在分裂中的小鼠卵母细胞中测试相关构造时发现,人工动粒能够与天然染色体动粒竞争微管结合,从而降低施加在染色体对上的整体拉力,使黏连性减弱的染色体对也更容易维持连接状态。
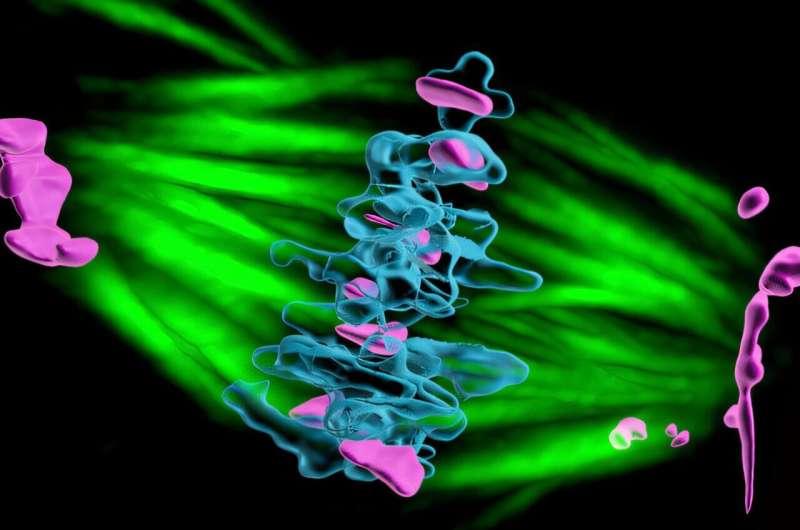
研究人员进一步展示了新一代人工动粒:由紧凑的蛋白质组装体构成,可在卵母细胞内直接表达。相关研究已发表于《自然细胞生物学》(Nature Cell Biology)。
减数分裂包含两个阶段,最终形成的配子仅含每条染色体的一份拷贝,而非体细胞中的两份。研究团队表示,其人工动粒策略可帮助老年小鼠卵母细胞在减数分裂两个阶段实现更正常的染色体DNA分配。
研究人员认为,这一方向未来或可为年长父母的健康受孕提供潜在治疗思路,但距离临床应用仍有较长路径。北岛表示,该策略离临床应用“还很遥远”,但未来存在实现可能。为推进相关研究,他计划开发更能反映人类卵母细胞生成复杂性的动物模型,用作测试人工动粒策略的实验平台。











