当多种致病细菌暴露于青霉素等β-内酰胺类抗生素时,并不一定会被立即杀灭,而可能进入一种被称为“抗生素耐受性”的暂时存活状态。在这一状态下,细菌能够承受通常足以致死的药物浓度。研究人员指出,耐受性不同于完全的抗生素抗药性,但被视为可能通向抗药性的风险信号。
研究绘制青霉素压力下的代谢图谱
由博士后研究员梅根·凯勒(Megan Keller)与高级作者、农业与生命科学学院微生物学副教授、韦尔细胞与分子生物学研究所成员托比亚斯·多尔(Tobias Dörr)领导的研究,首次系统揭示了细菌在高剂量青霉素作用下维持存活所依赖的代谢变化,并识别出其存活机制中的潜在薄弱环节。相关论文发表于《npj抗微生物剂与抗药性》。
研究以霍乱弧菌(Vibrio cholerae)为模型。多尔表示,细菌在青霉素存在期间会停止分裂,但仍保持代谢活跃并存活;当抗生素压力解除后,细菌可恢复生长并继续造成感染。
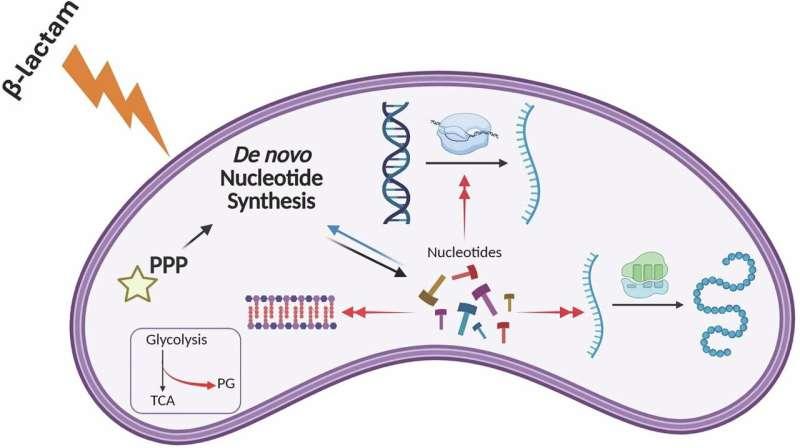
为解释细菌如何在强烈药物压力下存活,研究团队一方面分析青霉素处理期间哪些基因被激活或抑制,另一方面测量细胞产生的数千种分子变化,从而构建了细菌在β-内酰胺类抗生素压力下内部变化的详细图谱。
核苷酸急剧下降成为“意外脆弱点”
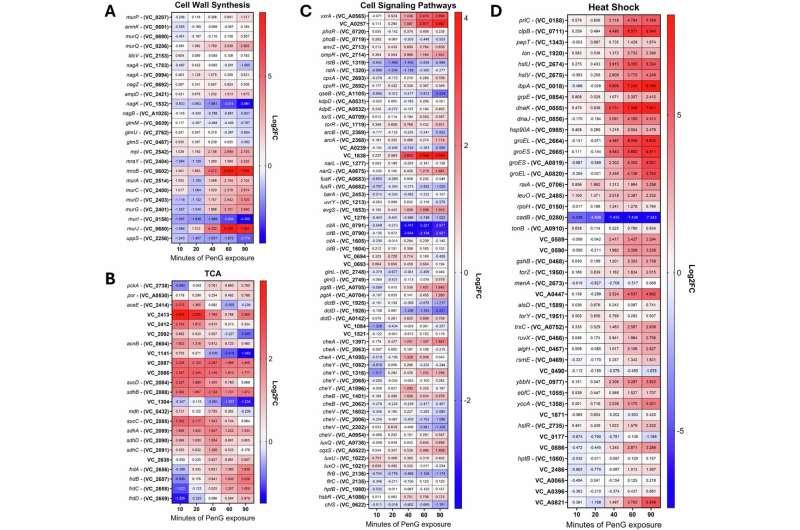
研究显示,部分变化符合预期:与细胞壁修复相关的基因活性增强,提示细菌试图修复药物造成的损伤;同时,合成核苷酸所需的嘌呤与嘧啶代谢途径活性也有所提高。
不过,多尔指出,最显著的变化是核苷酸水平出现急剧下降。核苷酸是DNA及其他关键细胞组分的重要前体,支撑多种基本细胞过程。
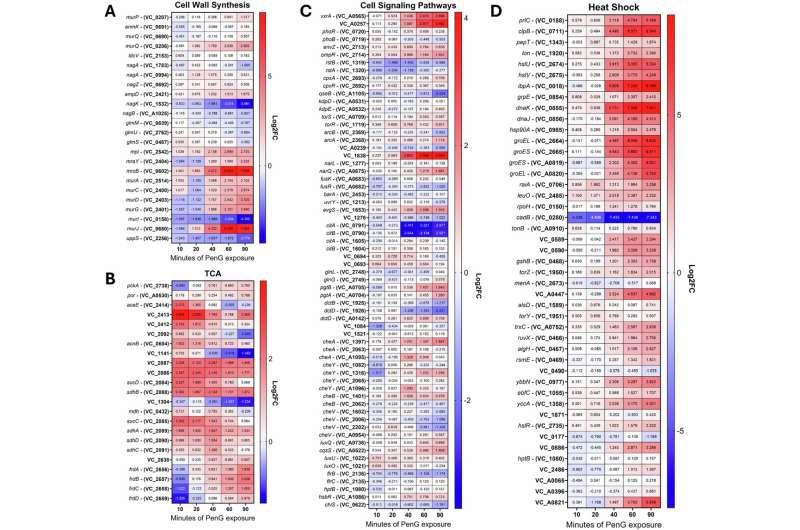
研究团队提出的机制解释是:细菌通常会分解糖类并将其分子子组分用于合成细胞壁材料、氨基酸和核苷酸等。青霉素会导致细胞壁合成过程失控,使大量葡萄糖被“挤占”到细胞壁合成通路,进而造成用于核苷酸合成的原料不足。
联合用药显著降低多种病原菌存活率
基于“核苷酸匮乏”这一代谢瓶颈,研究进一步提出并验证了一个问题:在细菌已处于核苷酸不足的情况下,若再阻断核苷酸合成,是否会使其更易被杀灭。
为此,团队将青霉素与已知可干扰核苷酸合成的药物甲氧苄啶(trimethoprim)联合用于处理霍乱弧菌。多尔称,单独使用任一药物仅能杀灭一定比例细菌,但两者联用使霍乱弧菌存活率下降超过10万倍。
研究还报告称,类似的强烈效果也出现在其他医学重要菌种中,包括与抗药性肺炎和尿路感染相关的肺炎克雷伯菌(Klebsiella pneumoniae),以及食源性致病大肠杆菌(E. coli)。
指向以“代谢瓶颈”为靶点的策略
研究人员表示,这一发现为应对抗生素耐受性提供了新的思路:未来策略或可不依赖提高抗生素剂量,而是通过联合使用能够利用青霉素诱发核苷酸短缺的化合物来增强杀菌效果。
多尔指出,在临床环境中,将甲氧苄啶等既有药物作为β-内酰胺类抗生素的辅助用药,可能具有现实可行性。尽管“鸡尾酒”式组合疗法在临床并不罕见,但针对“核苷酸合成抑制”与β-内酰胺类抗生素的特定联用思路,尚未成为常规方向。











