研究人员在原子水平上解析了一种细菌构建三维(3D)生物膜的关键机制,显示包括鲍曼不动杆菌与铜绿假单胞菌在内的病原体可借此形成对抗生素更具耐受性的生物膜结构。相关研究已发表在《自然通讯》(Nature Communications)。
多种致病细菌会形成三维生物膜,以降低免疫系统清除、抗生素治疗以及环境表面干燥等因素带来的影响。在医院环境中较为棘手的多药耐药菌株,如鲍曼不动杆菌和铜绿假单胞菌,能够利用一种称为粘附菌毛的毛状丝状结构附着于组织或非生物表面。附着后,细菌继续增殖并逐步形成由多层细胞构成的厚实三维生物膜。尽管该过程同样由粘附菌毛介导,但此前菌毛如何在生物膜生长过程中维持结构稳定、避免解体仍不清楚。
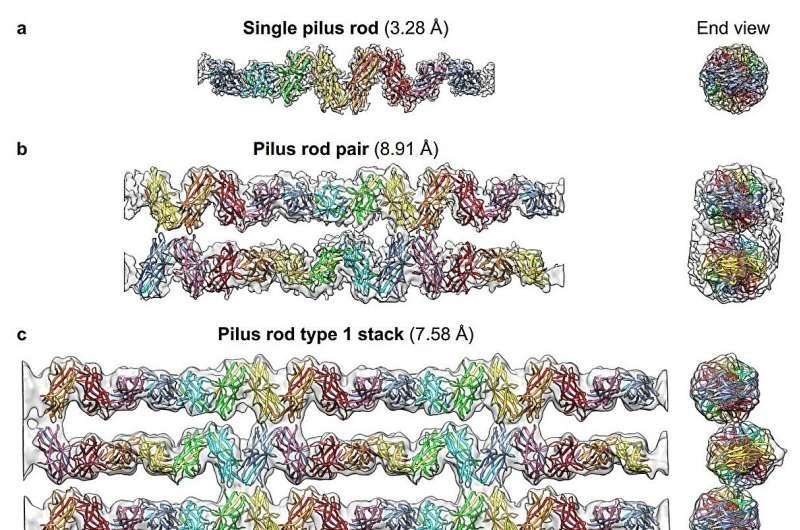
芬兰图尔库大学MediCity研究实验室团队借助先进电子显微镜技术发现,邻近鲍曼不动杆菌的粘附Csu菌毛可通过反平行方式相互连接,并快速自组装为扁平片状结构,从而将细菌细胞连接成网络并提升其在不利环境中的存活能力。该研究由高级研究员Anton Zavialov领导。
Zavialov表示,Csu菌毛能够自组装成规模庞大且复杂的网络结构,可连接数百个细菌细胞。研究团队进一步证明,Csu菌毛至少可形成两种类型的扁平结构,并以近原子分辨率对其进行了结构解析。
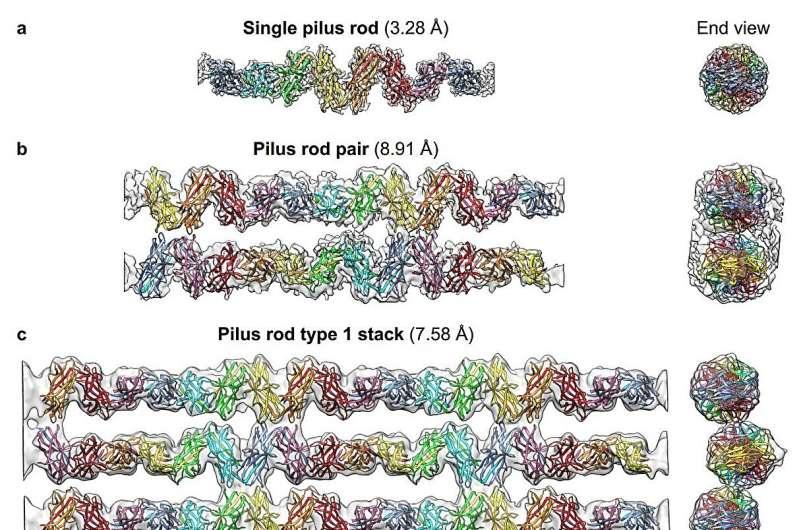
第一作者、博士研究员Henri Malmi介绍,冷冻电子显微镜技术近年来发展迅速。为获得首个结构模型,他起初采用手动方法,随后再结合计算工具处理这些体量异常庞大的三维组装结构。
研究还显示,菌毛网络嵌入在由细菌分泌的多糖与DNA构成的相对不规则基质中。Zavialov将其比作“钢筋混凝土”结构:菌毛类似钢筋,多糖与DNA则形成“混凝土”,使细菌得以隐藏在更具防护性的结构之中。
研究团队表示,目前正尝试开发针对菌毛连接部位的抑制剂。相关抑制剂有望用于联合疗法,以阻断三维生物膜的组装过程,从而帮助抗生素更有效地清除病原体。











