神经嵴细胞是一类在胚胎早期发育阶段迁移并进入多种组织的干细胞群体。研究显示,这些细胞参与形成眼睛与皮肤的色素以及面部骨骼结构;在体内,它们还构成外周神经系统的髓鞘,并形成肠道的肠神经系统,后者常被称为“第二大脑”。
与神经嵴细胞迁移异常相关的疾病被统称为神经嵴病。其中较常见的是Hirschsprung病,发病率约为每5000名新生儿中1名。该病患儿结肠缺乏神经系统,被认为与胚胎发育过程中神经嵴细胞未能完全到达消化道末端有关。报道指出,如出生时不进行手术治疗,该病可致命,且超过一半病例的病因仍不明确。
在已知与Hirschsprung病相关的基因中,肽类内皮素3(endothelin-3)及其受体EDNRB长期受到关注。报道提到,携带内皮素3或EDNRB基因缺陷的小鼠和人类可出现相关疾病表现,部分病例还伴随色素沉着或颅面缺陷。内皮素最初在20世纪80年代被发现为血管内皮分泌的血管收缩物质,可促使血管平滑肌收缩并参与血压调节。
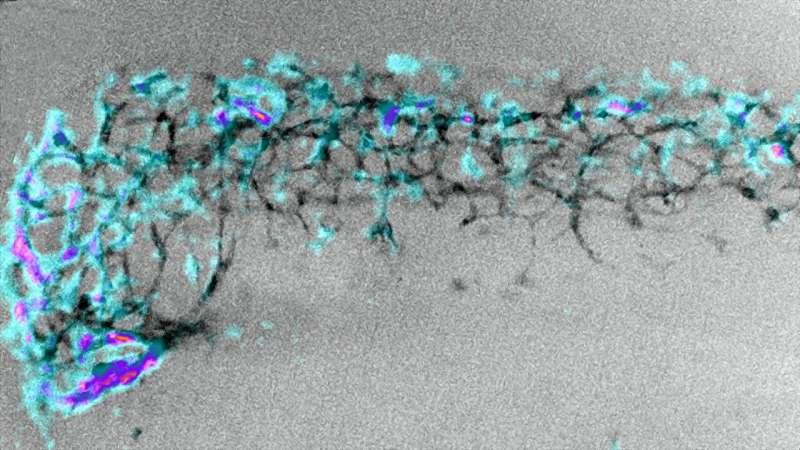
研究人员在2022年与雅克·莫诺研究所的同事合作,构建了在神经嵴细胞中表达钙荧光报告蛋白的小鼠品系。根据研究描述,当细胞出现电活动时,细胞内钙水平上升并引发荧光闪烁。研究团队在观察到迁移至肠道的细胞出现钙信号闪烁后,进一步测试多种与Hirschsprung病相关的蛋白,其中内皮素3引发的反应最为显著:可在细胞网络中触发一波强烈的钙信号传播。
研究团队随后指出,肠道神经嵴细胞的大部分“自发”钙活动,可能来源于胚胎肠组织自然产生的内皮素3;当阻断其受体EDNRB时,这类活动几乎完全停止。研究还称,内皮素3与EDNRB结合后,可开启氯离子通道与T型钙通道,导致细胞内钙呈振荡性流入。
在对相关离子通道进行阻断或刺激的实验中,研究人员观察到神经嵴细胞迁移出现缺陷或增强的变化。报道同时提到,近期一项全基因组筛查发现,T型钙通道突变可导致Hirschsprung病,提示电活动与神经嵴细胞侵入结肠的能力存在关联。
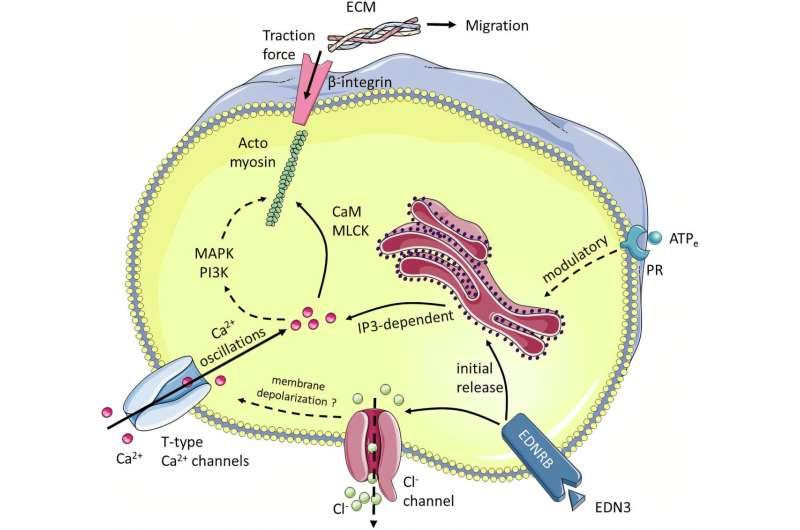
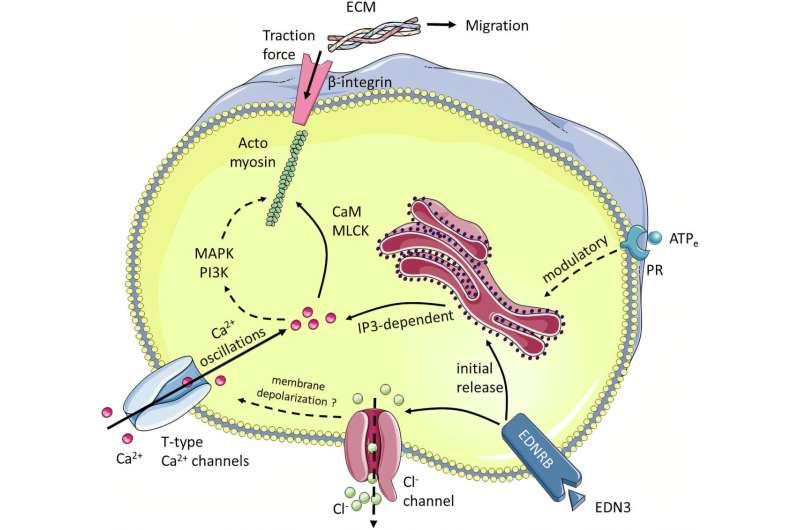
为解释钙活动如何提升细胞运动能力,研究人员将机制与血管平滑肌的收缩过程进行对照:在血管平滑肌中,内皮素可通过开启离子通道引发钙流入并激活收缩机制。研究团队据此提出,尽管神经嵴细胞并非肌肉细胞,但细胞内普遍存在一定量的肌动蛋白-肌球蛋白体系,可能同样产生收缩样行为。
在验证实验中,研究人员将细胞置于易变形的胶原凝胶中,并在凝胶内嵌入纳米级荧光微珠,用以记录细胞迁移时对凝胶纤维的牵引与形变。研究结果显示,内皮素3可作为肠神经嵴细胞的“收缩剂”,帮助其产生更大拉力以穿越肠道组织;而EDNRB阻断剂则产生相反效果,使牵引力减弱。
研究团队在发表于《自然通讯》的论文中据此认为,神经嵴细胞在定殖胚胎肠道过程中表现出类似“微型肌肉”的特征,通过电活动相关的钙信号触发收缩样牵引力,从而影响迁移与定殖。报道指出,这一机制为神经嵴病的诊断提供了新的线索:凡参与神经嵴电活动或收缩活动的蛋白发生突变,均可能导致迁移缺陷并引发相关病理。
报道还提到,黑色素瘤和胶质母细胞瘤被认为与侵袭性神经嵴细胞发育程序的再激活有关,研究团队认为其揭示的机制可能同样作用于转移过程,并为肿瘤相关药物开发提供潜在思路与靶点。
该研究作者之一Nicolas R. Chevalier为法国国家科学研究中心(CNRS)生物物理学家,任职于巴黎城市大学复杂物质与系统实验室(MSC),其研究方向涵盖肠道发育与生理等领域。











