纽约大学阿布扎比分校(NYU Abu Dhabi)研究人员开发了一种基于光的纳米技术,旨在改进部分癌症的检测与治疗,并为化疗、放疗及手术提供更精准、潜在危害更小的替代路径。相关成果已发表于《Cell Reports Physical Science》。
研究团队围绕光热疗法(photothermal therapy)展开工作。该疗法通过光照在肿瘤内部产生热量,以破坏癌细胞。研究人员设计了微小的生物相容、可生物降解纳米颗粒,颗粒携带一种可被近红外光激活的染料;当暴露于近红外光时,颗粒升温以破坏肿瘤组织,同时尽量减少对健康细胞的影响。团队选择近红外光的原因在于其相较可见光具有更强的组织穿透能力,从而可用于治疗不靠近体表的肿瘤。
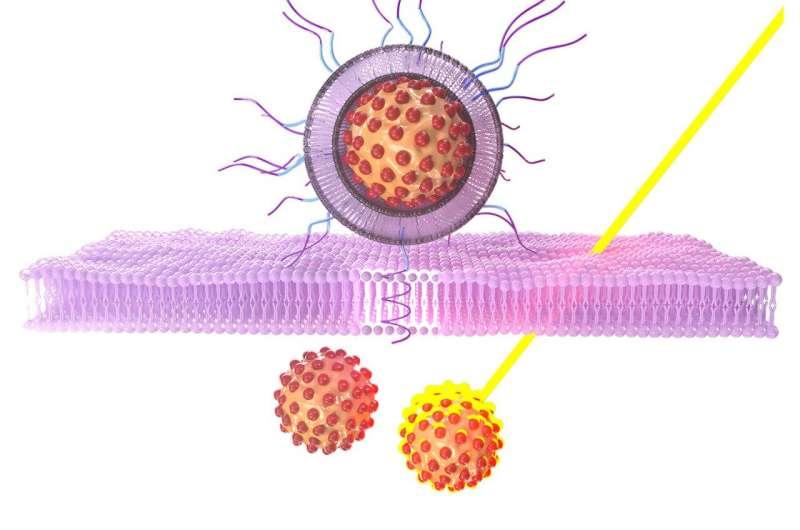
研究指出,光热疗法面临的关键挑战之一,是在体内维持光响应材料的稳定性并实现高效肿瘤递送。部分现有光热剂可能出现降解较快、从血液中被清除或难以高效进入癌细胞等问题。
为应对上述难点,研究人员开发了以羟基磷灰石为核心材料的纳米颗粒。羟基磷灰石是一种存在于骨骼和牙齿中的矿物质。团队在颗粒表面包覆脂质和聚合物,以延长其在血液中的循环时间并降低被免疫系统识别的概率,从而使更多治疗材料到达肿瘤部位。与此同时,颗粒利用肿瘤微酸性环境的特征:其表面的一种肽在该环境下被激活,帮助纳米颗粒更高效进入癌细胞,并在较大程度上避免进入健康组织。
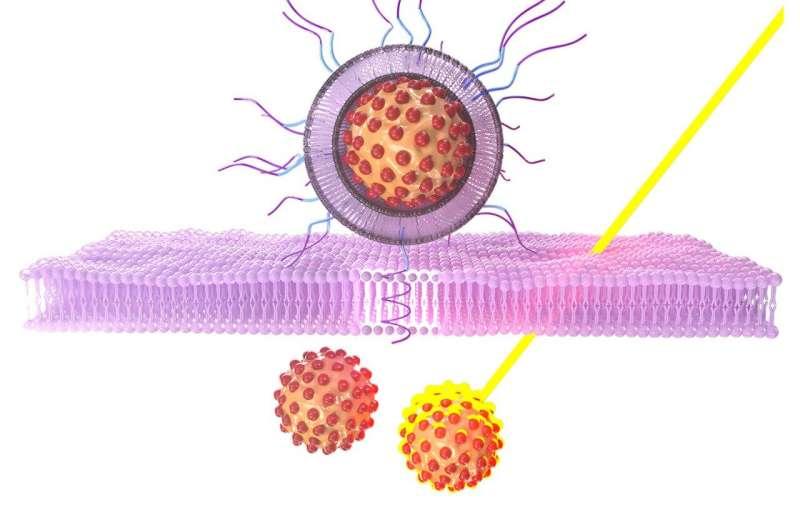
研究人员表示,这些纳米颗粒表现出较高稳定性,能够有效保护染料不被降解,并可在肿瘤部位实现高效积聚。在近红外光激活后,颗粒产生局部热量以破坏肿瘤组织,同时产生荧光与热信号,用于肿瘤可视化并支持对治疗效果的实时监测。
该研究资深作者、纽约大学阿布扎比分校生物学副教授马津·马格祖布(Mazin Magzoub)表示,这项工作将靶向治疗与成像整合到一个生物相容且可生物降解的系统中,并通过解决治疗剂递送至肿瘤的关键挑战,提升癌症治疗的精准度。
研究结果显示,该纳米颗粒具备作为癌症诊断与治疗一体化系统的潜力,为更安全、更有效的基于光的癌症治疗提供了新的技术方向。











