多种蛋白质因其复杂三维结构而具备特定生物功能,外源分子若能结合到蛋白质的特定位点,可能改变其功能。亥姆霍兹中心柏林(HZB)团队近期围绕SARS-CoV-2感染过程中发挥作用的Nsp1蛋白开展结构研究,并在BESSY II同步辐射装置上完成第5000个蛋白质结构解析。
HZB表示,尽管由SARS-CoV-2引发的全球大流行已减退,但多种变异株仍在全球传播,相关有效药物的研发工作仍在推进。此次研究聚焦于Nsp1蛋白的主结构域。研究团队指出,Nsp1可阻断宿主细胞核糖体中宿主自身蛋白的合成,从而削弱宿主对SARS-CoV-2的防御,因此其主结构域被视为抗病毒药物开发的潜在靶点。
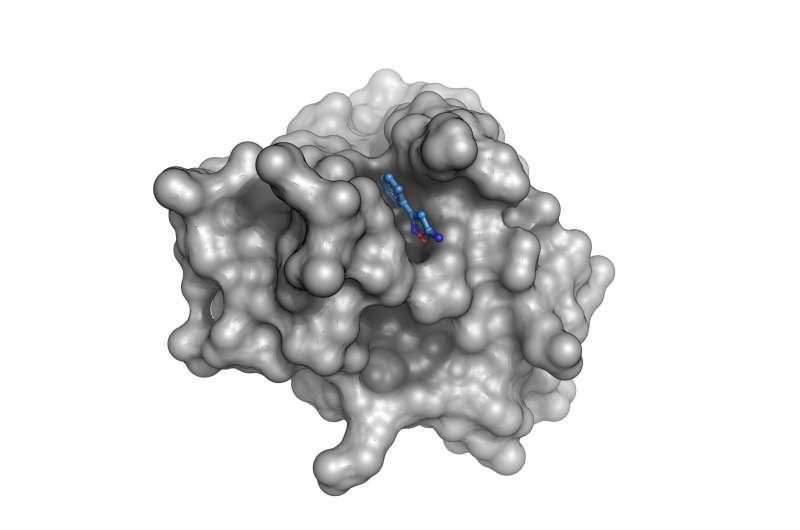
在实验方法上,BESSY II的MX团队采用片段库进行高通量筛选。该片段库包含数百种小分子,研究人员将每一种小分子分别与Nsp1蛋白晶体混合,随后在BESSY II的MX光束线上对晶体进行测量并解析对应的三维结构。
研究结果显示,共有21种小分子能够与Nsp1主结构域结合。团队进一步观察到,多种片段(包括第5000个结构中呈现的片段)可深入嵌入Nsp1在功能重要区域附近的一个口袋。
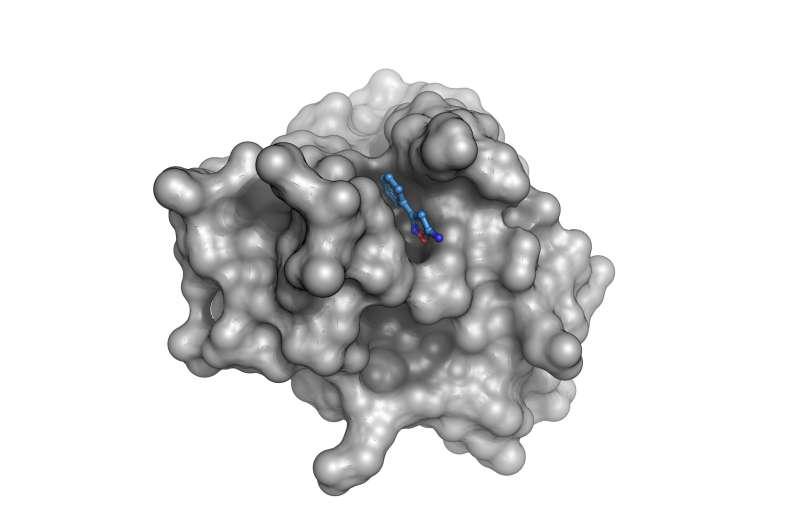
论文第一作者Frank Lennartz博士表示,这些发现为开发更大的药物分子提供了起点,相关分子有望在SARS-CoV-2复制过程中干扰Nsp1。HZB大分子晶体学负责人Manfred Weiss博士称,片段筛选可系统测试小型化学构建块并识别其与蛋白质特定位点的结合情况,从而揭示蛋白质的“脆弱点”,并为后续开发更复杂的活性物质提供起始模块。
上述研究已发表在《Acta Crystallographica Section D Structural Biology》。
发表评论
登录后才可评论。
去登录











