细胞会将分子组织到不同的功能区域。除线粒体、细胞核等传统有膜细胞器外,近年来研究还确认了应激颗粒、蛋白酶体储存颗粒(PSGs)等无膜细胞器的存在。
过去,这类无膜结构多依赖荧光显微镜观察,通常呈现为“液滴”样信号。来自马丁斯里德马克斯·普朗克生物化学研究所、哥廷根大学医学中心和多伦多大学的研究团队此次利用冷冻电子断层扫描技术,在细胞内解析了PSGs的分子级结构细节。相关成果已发表于《Cell》。
蛋白酶体是一种大型蛋白复合物,可在能量驱动下将特定不需要或受损的蛋白质切割为小片段,从而实现清除。蛋白酶体存在于从酵母到人类的所有真核生物中,并被认为对生命活动至关重要。研究人员指出,蛋白酶体也与肿瘤细胞对部分抗癌药物的反应相关;在营养物质或其他能量来源不足时,细胞内蛋白酶体的定位会发生明显变化。
马克斯·普朗克生物化学研究所所长布伦达·舒尔曼表示,与冷冻电子断层扫描领域研究者沃尔夫冈·鲍迈斯特的合作,使团队能够在分子层面理解PSGs的功能。她指出,许多分子机器会组装成无膜细胞器,而要理解其功能,需要看到其分子结构。
在研究中,团队通过剥夺酵母细胞葡萄糖或阻断线粒体ATP生成,使细胞处于能量压力状态并出现ATP匮乏。PSG研究人员科杜拉·埃嫩克尔解释,细胞在这种情况下会将蛋白酶体排列成PSGs,以关闭高能耗的蛋白酶体活动。多伦多大学结构生物学家奥利弗·恩斯特补充称,理解PSGs结构对阐明细胞应对代谢压力的策略至关重要,但仅依靠纯化蛋白酶体无法实现这一目标。
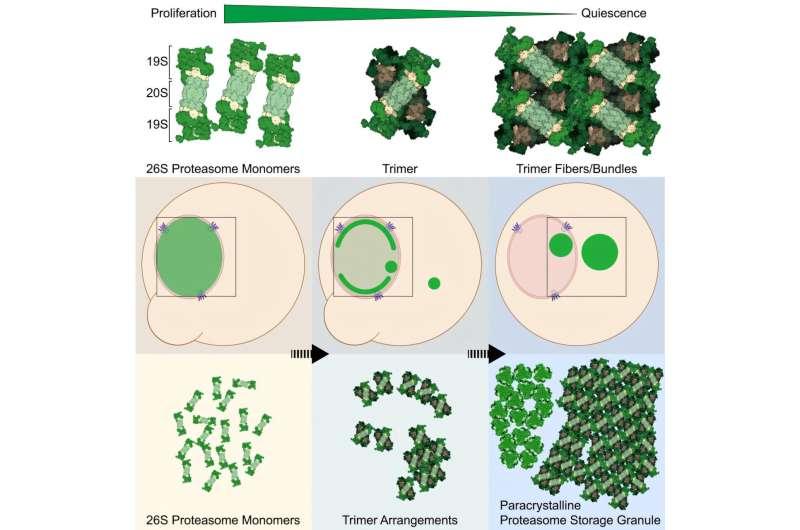
研究第一作者之一唐晓萌介绍,团队在蛋白酶体储存颗粒的自然环境——细胞内——进行观察。冷冻电子断层扫描使研究人员以0.9纳米分辨率成像PSGs,首次看到单个蛋白酶体以精确、重复的方式排列成晶体状结构。研究人员表示,这一结果与此前关于PSGs可能以无定形簇或动态液滴方式组装的设想不一致。
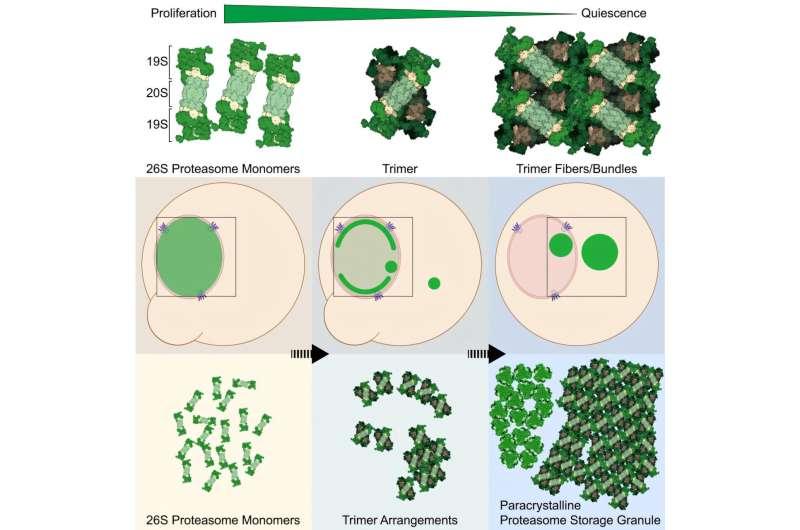
团队进一步解析了PSGs的组装过程:蛋白酶体首先形成三聚体,即三个蛋白酶体结合在一起;随后三聚体堆叠形成纤维,纤维再进一步结合形成束状结构。研究人员称,这种三聚体结构此前未在细胞中被观察到。
共同第一作者曲璐表示,这种排列只能在细胞内被展示,难以在体外重现;当研究人员尝试分离PSGs时,其结构会解体,因此冷冻电子断层扫描成为关键技术。研究显示,在酵母细胞中,PSGs可保持完全组装但处于非活跃状态,从而在能量短缺时避免额外能量消耗。
曲璐还指出,蛋白酶体通过特定的蛋白质—蛋白质相互作用维持非活跃状态,形成的准晶体结构稳定但可被破坏,使蛋白酶体在能量来源恢复后能够迅速重新激活。研究人员向饥饿细胞补充葡萄糖后,蛋白酶体在一小时内恢复到正常功能结构。
舒尔曼表示,这一发现为无膜细胞器的形成提供了新的视角,即通过分子机器结构良好的区域之间的接触形成,从而使PSGs能够在细胞条件不利时安全储存制造成本高且必不可少的蛋白酶体,并在条件改善时快速投入使用。鲍迈斯特则表示,在细胞天然环境中研究蛋白酶体等结构,有助于从根本上改变对细胞组织与功能的理解。











