德国哥廷根大学医学中心(UMG)牵头的国际研究团队利用高分辨率电子显微成像,在接近天然的细胞环境中捕捉到线粒体在压力条件下维持功能的关键分子过程。研究显示,线粒体热休克蛋白60(mHsp60)这一帮助蛋白质获得功能构象的“折叠助手”,会在压力下重塑自身结构,从而提升活性,支持线粒体蛋白质折叠与功能维持。
相关成果已发表于《Science Advances》。研究团队表示,这一发现有助于进一步厘清与帕金森病等严重神经退行性疾病相关的细胞过程。
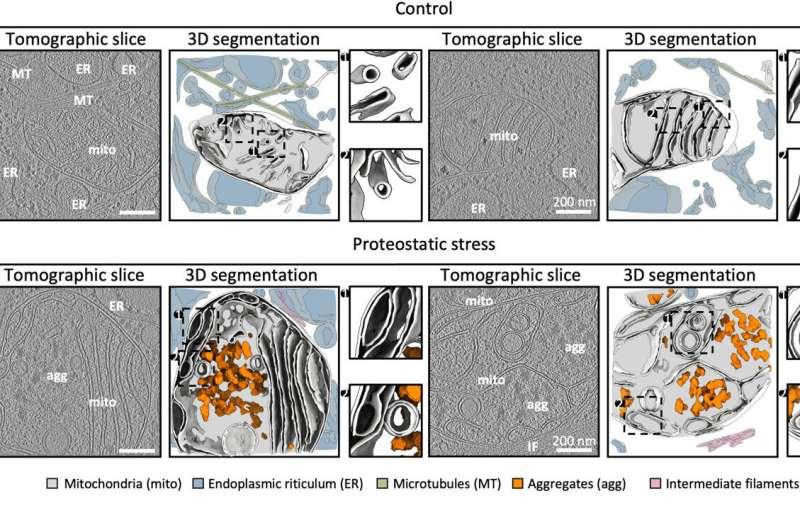
线粒体承担细胞内大部分能量生成任务,因此肌肉与大脑等高能量需求组织对线粒体功能障碍更为敏感。研究介绍,中脑中主要产生并释放神经递质多巴胺的多巴胺能神经元对能量需求尤高;多巴胺参与动机、运动、情绪与驱动力等功能,而这些神经元在帕金森病中会出现选择性退化,但其潜在机制仍未完全明确。根据帕金森欧洲组织数据,帕金森病影响全球超过1000万患者,目前尚无治愈方法。
研究人员提出,一种可能情形是多巴胺能神经元的高能量需求使其线粒体长期承受异常压力,进而导致线粒体功能失调。与此同时,研究也提到,在某些癌症类型中,线粒体健康水平的增强可能提升癌细胞增殖能力。因此,理解线粒体健康维持与压力抵抗的分子机制被认为具有重要意义,但此前受限于技术条件,科学界难以在细胞内以足够分辨率直接观察相关过程。
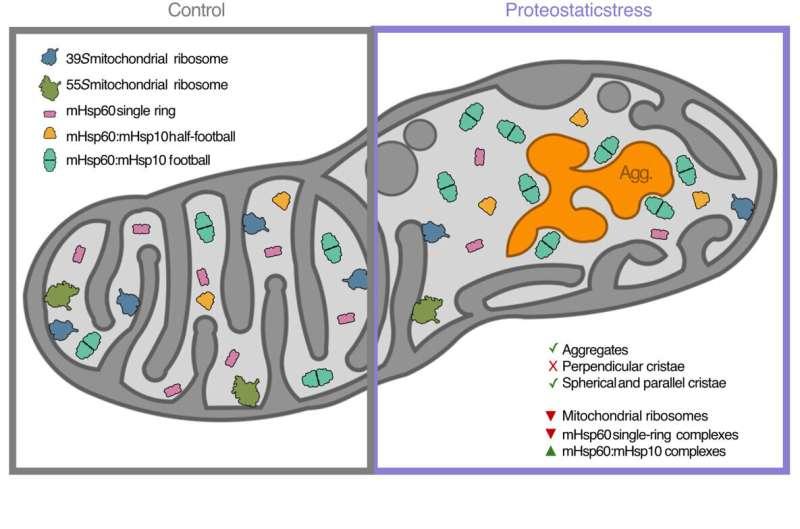
本研究由哥廷根大学医学中心神经病理学系“结构细胞生物学”工作组负责人、哥廷根多尺度生物成像卓越集群(MBExC)成员Rubén Fernández-Busnadiego教授领导。团队采用冷冻电子断层扫描(cryo-electron tomography)对经超快速冷冻的三维细胞进行成像,使细胞结构保持在接近天然状态,并以近原子精度呈现线粒体在压力下的应对方式,包括下调蛋白质翻译以及增强蛋白质折叠这一确保蛋白功能性的关键过程。
研究进一步锁定mHsp60为线粒体压力条件下维持功能的关键蛋白,并以高分辨率展示其工作机制:mHsp60在压力环境中形成更多复合体,通过将底物蛋白封装在保护性的桶状结构内促进正确折叠;同时,其三维结构发生改变,使其在严苛压力下仍能持续并增强地完成线粒体蛋白质折叠。
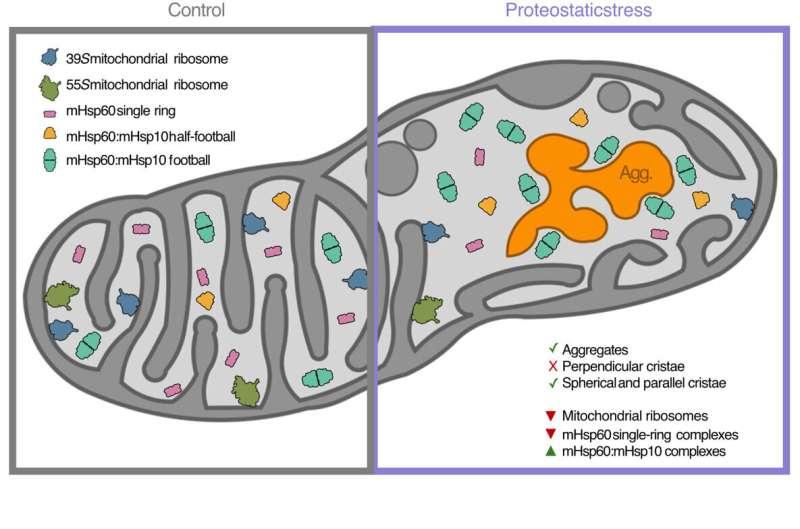
Fernández-Busnadiego表示,团队在细胞“能量工厂”内进行压力测试,旨在解析质量控制的分子机制及其薄弱环节,并重点关注细胞压力、蛋白质错误折叠与严重神经退行性疾病之间的联系。第一作者、UMG神经病理学系博士后研究员、MBExC教学培训平台Hertha-Sponer-College成员Kenneth Ehses指出,冷冻电子断层扫描使研究人员能够在天然细胞环境中直接研究蛋白质复合体,从而探究疾病发展的可能机制;他同时表示,这些发现有望推动帕金森病等神经退行性疾病新治疗策略的开发。
在实验设计上,团队对人类细胞施加线粒体压力,随后将样本在约-200摄氏度条件下快速冷冻并进行成像。研究称,压力由一种化学物质诱导,该物质会导致线粒体内错误折叠且失活的蛋白质积累,从而触发mHsp60复合体增加形成。成像结果不仅呈现桶状结构在人体细胞中的组装方式,也揭示mHsp60结构变化与其在压力下维持折叠能力增强之间的关系。
研究团队表示,mHsp60的功能与结构循环分析是在与西班牙Biofisika研究所、以色列特拉维夫大学以及英国邓迪大学研究人员合作下完成。下一步,团队计划研究该循环在包括帕金森病在内的病理条件下如何发生变化。











