美国研究人员借助一种改良的荧光显微与光谱测量方法,获得了大型蛋白质分子如何快速、稳定折叠成特定三维结构的更细致观测结果。美国国立糖尿病、消化及肾脏疾病研究所(NIDDK)的钟海松(Hoi Sung Chung)及其同事在论文中指出,蛋白质折叠可能并非由单一区域依次完成,而是由分子多个部分以更协调的方式共同推进。相关成果发表于《物理评论快报》(Physical Review Letters)。
蛋白质折叠问题仍待破解
蛋白质是生命系统中关键的大型复杂生物分子。在未折叠状态下,蛋白质通常表现为长而无序的氨基酸链,但会在极短时间内折叠为特定的三维结构,而这一结构与其生物功能密切相关。
研究人员指出,蛋白质折叠不仅速度极快,往往在毫秒的千分之一量级内完成,而且具有高度可靠性:尽管同一条氨基酸链理论上可采取大量不同构象,其中多数并不具备功能,但蛋白质几乎总能折叠到相同的功能性结构。这一现象表明,最终形状在很大程度上由氨基酸序列所编码。
不过,氨基酸序列如何在不穷尽所有可能构象的情况下,引导分子快速且可靠地到达正确结构,仍存在诸多未解之处。这一被称为“蛋白质折叠问题”的难题,是生物物理学的核心挑战之一。
纳米光子波导增强荧光信号
为获取折叠过程的更多细节,钟海松团队开发了增强型荧光测量方案:研究人员先用有机染料对蛋白质样本进行标记。在传统荧光技术中,染料在特定波长光照下被“荧光团”吸收能量,随后发射出不同波长的光;通过统计发射光子,研究人员可推断染料位置,从而以纳米级精度描绘蛋白质结构。
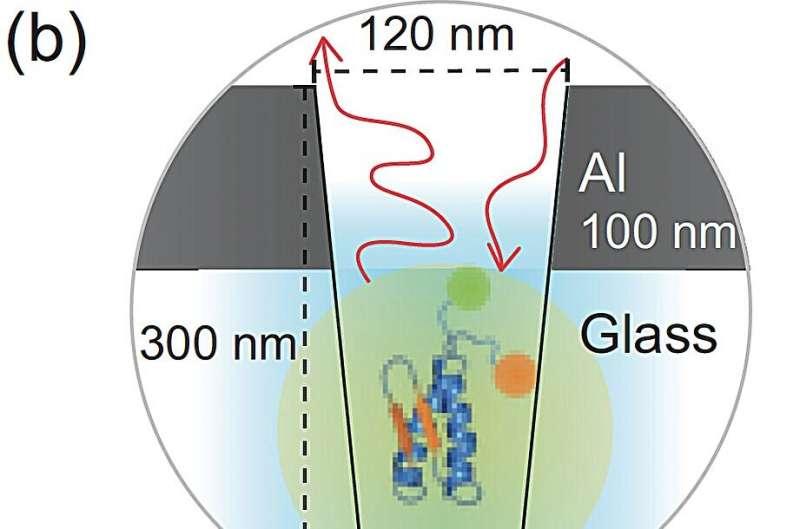
研究团队表示,蛋白质折叠事件发生极快,若荧光信号不足,往往难以在折叠完成前积累到足够清晰的数据,从而影响测量可靠性。为此,他们将蛋白质分子置于溶液中,使其在折叠与未折叠状态之间不断切换,并将标记后的溶液引入一种纳米光子波导结构。
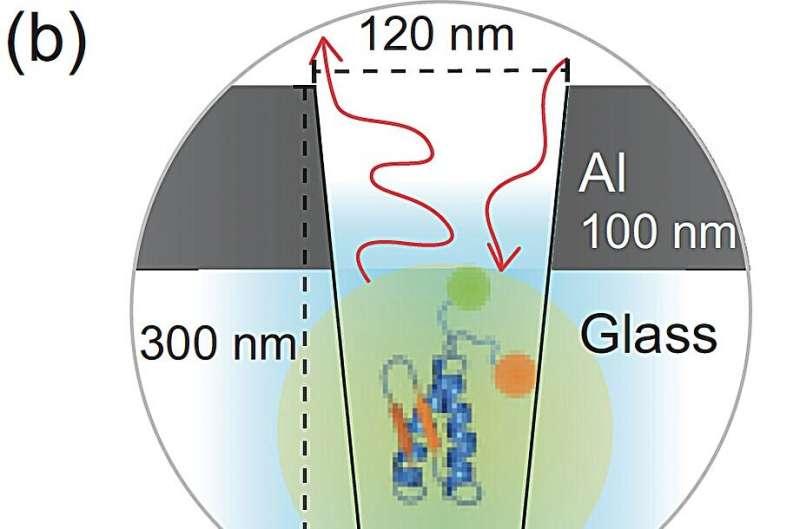
该波导结构可增强荧光团的发射强度,使其在每微秒释放更多光子,从而让研究人员能够在极短时间尺度内记录到更完整的分子信号。
折叠转变发生在0.7至4微秒
根据论文报告,测量结果显示,蛋白质的折叠转变发生在约0.7至4微秒的时间尺度内。研究团队同时观察到一个出乎预期的现象:较大的蛋白质似乎比小型蛋白质更容易完成这一转变。
为解释这一结果,研究人员提出,大型蛋白质分子的多个区域可能会同时开始形成最终结构,这种“协调折叠”有助于使整体折叠过程更顺畅,从而更高效地到达最终构型。
论文还提到,研究团队认为这种行为可能在数百万年的进化过程中逐步形成,使蛋白质能够在众多可能的折叠路径中进行探索,并最终选择更有效的路径。











