非对映异构体是结构相同但并非镜像关系的一类分子。由于不同非对映异构体可能在生物活性、效力或毒性等方面表现不同,且往往能够彼此分离,如何定向获得目标非对映异构体一直是有机合成中的重要难题。
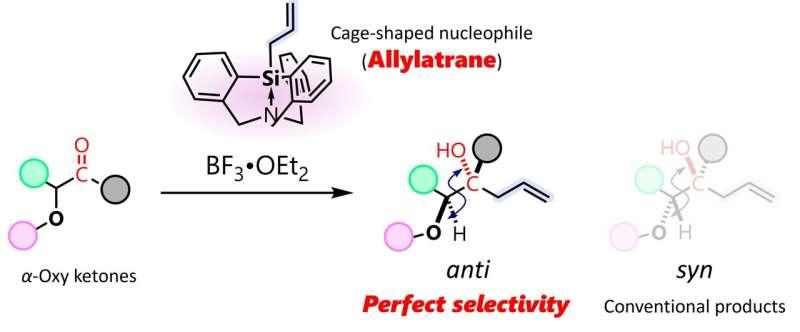
大阪大学研究团队近日报告了一种可提高特定非对映异构体生成比例的新方法,用于合成在传统反应条件下通常难以大量获得的产物。相关研究发表在《自然通讯》(Nature Communications)。
研究围绕药物与天然产物合成中常见的“构建模块”展开。其中,羰基由碳原子与氧原子通过双键连接;而α-氧羰基结构中,连接在羰基上的α-碳还带有含氧取代基。由于氧原子对电子的吸引作用,羰基碳呈现较强亲电性,富电子的亲核试剂可通过提供电子对与其发生加成,形成新的化学键。
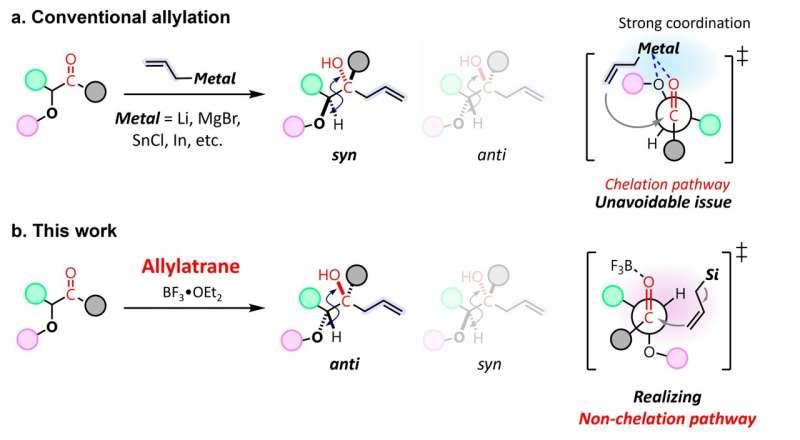
在该类反应中,烯丙基作为一种常用亲核试剂,可对α-氧羰基化合物发生加成,并可能形成两种非对映异构体:加成发生在α-氧取代基对侧时得到顺式加成产物,发生在同侧时得到反式加成产物。研究指出,由于α-氧基团具有较强的螯合倾向,反应通常更偏向生成顺式加成产物,从而使反式非对映异构体的产率偏低。
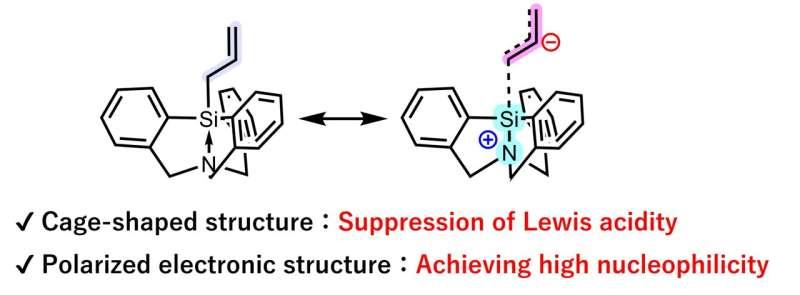
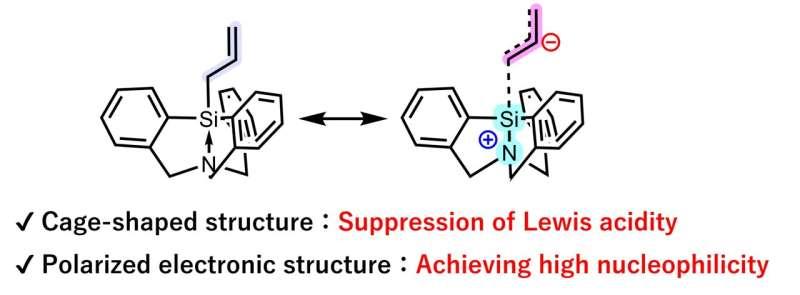
大阪大学团队在研究中实现了烯丙基对α-氧羰基化合物的反式加成,并使反式非对映异构体成为主要产物。第一作者筒井悠也表示,团队选用了一种具有笼状结构的烯丙基试剂——烯丙基三嗪。该分子中,多数原子连接在第14族中心原子(如碳或硅)上,高配位特征使其表现出很强的亲核性。
研究团队进一步称,烯丙基三嗪的刚性结构以及较低的路易斯酸性,使其不易与α-氧羰基底物形成更常见的顺式加成产物,从而改变了反应选择性,使反式非对映异构体成为主要生成物。资深作者安田诚表示,该策略可适用于多种底物,且反式非对映异构体的产率明显高于传统方法。
研究人员认为,该方法有望帮助在制造环节中更高比例获得过去往往仅以少量副产物形式出现的化合物,并可能成为合成用于药物及其他生物活性物质制造的独特分子的一项关键技术。











