新加坡国立大学(NUS)研究人员开发了单细胞分析框架CellScope,利用流形拟合方法处理单细胞RNA测序(scRNA-seq)数据,以构建更细致的“细胞图谱”,用于刻画不同细胞类型及其进一步细分的亚型。
随着单细胞图谱数据规模扩大、结构更为复杂,研究团队指出,部分现有分析工具在噪声背景下难以提取稳定的生物学信号,也难以刻画细胞组织的动态与层级特征。这些方法往往依赖单层次基因标记与有限的聚类分辨率,从而限制了对细胞类型如何分支为更专门亚群的探索。
CellScope由NUS统计与数据科学系姚志刚副教授团队牵头开发,目标是在多个聚类层次上生成高分辨率的细胞图谱。该框架基于一种建模思路:尽管每个细胞在数千个基因维度上被测量,但细胞间具有生物学意义的差异通常可由更低维度的内在结构(流形)来描述。与此同时,测量数据会受到两类噪声影响,包括在几乎所有细胞中活跃但难以区分细胞类型的管家基因,以及测序过程带来的技术噪声。
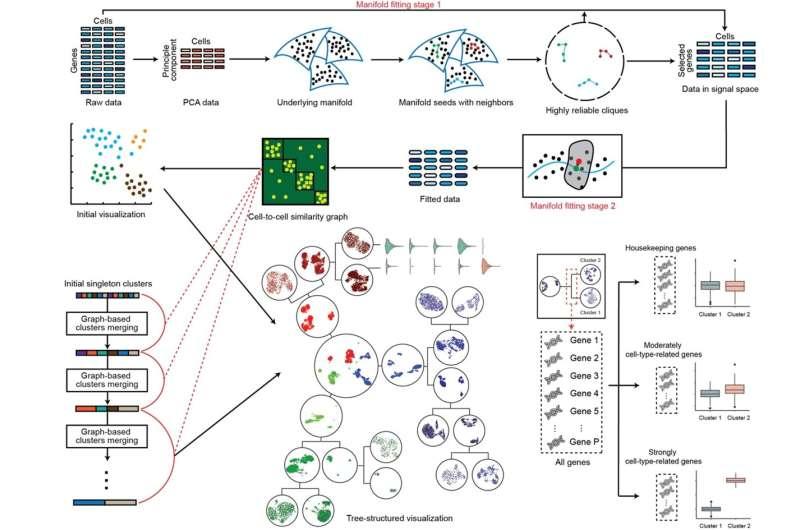
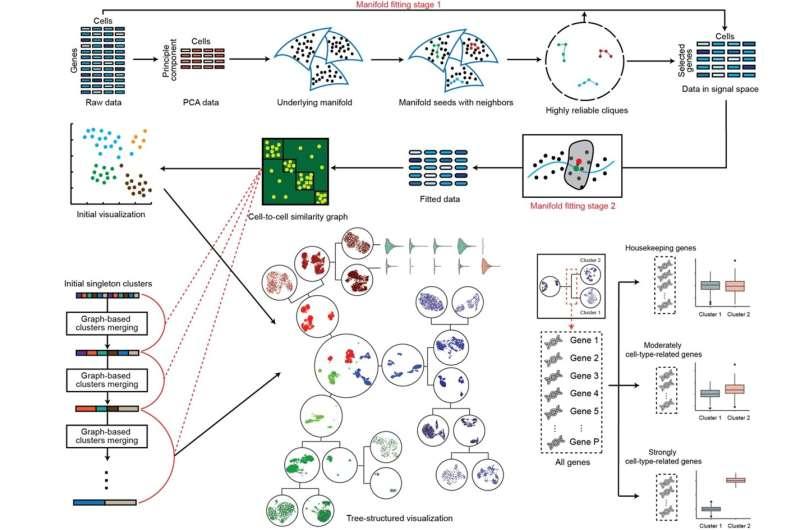
在方法设计上,CellScope采用两阶段流程:首先进行基因选择,以区分生物学信号与由管家基因驱动的变异;随后构建去噪的细胞表示,以提升紧密相关细胞群体之间的可分离性。该研究与华盛顿大学弗雷德哈钦森癌症中心Jessica Li教授合作完成。
研究团队表示,CellScope将多项关键组件整合为一体,包括自适应基因选择、基于流形结构的去噪、多分辨率层级聚类,以及以树状图展示聚类关系的可视化模块。框架还引入动态“分子身份”系统,用于跟踪基因在不同聚类层次上的重要性变化,而非将基因简单划分为“标记基因”或“非标记基因”。
在评估方面,CellScope在来自人类与小鼠模型组织的36个单细胞数据集上进行了测试。研究团队称,与多种常用工具相比,CellScope更频繁地产生与已知细胞标签一致的结果,并且不需要大量手动微调。
除性能评估外,研究人员还报告了该框架在生物学发现中的应用案例:CellScope识别出COVID-19患者血液样本中免疫细胞的变化,并显示该变化会随疾病严重程度增加而更为明显。
姚志刚表示,CellScope并非在既有工具上的渐进式改良,而是建立在流形拟合理论基础上的新框架;通过将几何理念引入单细胞分析,框架用于估计复杂生物数据背后的内在低维结构,并在准确性、计算效率与可解释性之间实现平衡,同时减少对人工调参的依赖。
上述研究成果已发表于《Nature Communications》,论文链接为:https://www.nature.com/articles/s41467-025-67890-3。研究团队还表示,未来将继续开发与维护CellScope,计划扩展其对空间转录组学与多模态组学等新兴数据类型的兼容性,并对大型公共数据集开展系统性再分析,以识别更多细胞亚型与疾病相关信号。











