微管由微管蛋白异二聚体连接形成空心圆柱结构,是细胞骨架的重要组成部分,在细胞内承受力与货物运输等过程中发挥作用。香港大学工程学院机械工程系林元教授与李嘉诚医学院生物医学科学学院戴杰夫教授领导的跨学科团队,报告了微管生物功能在微管蛋白层面可通过机械调控实现的新证据。
研究团队指出,微管在执行功能时需要与多类蛋白质相互作用:部分蛋白质可结合在微管外表面,另一些则在微管腔内与内表面发生作用。相较外表面易于接触,腔内结合蛋白如何进入微管受限的内表面,以及微管晶格如何决定腔内可达性的分子机制,长期缺乏清晰解释。
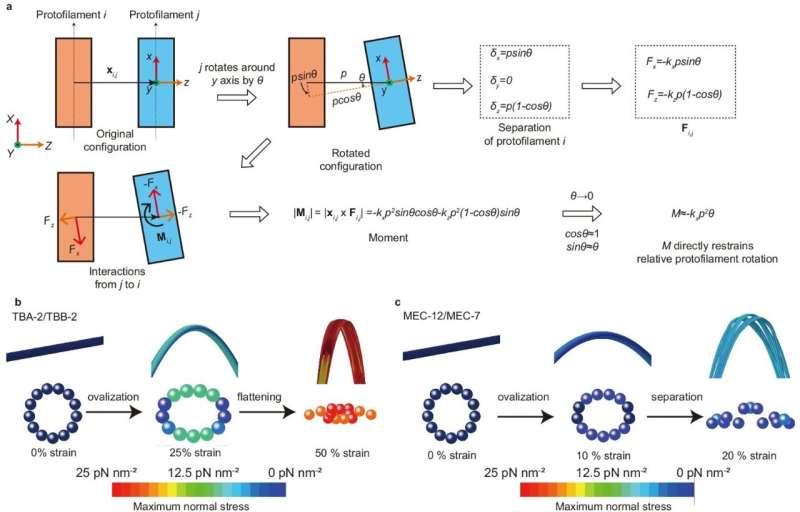
据介绍,戴杰夫团队首次将基于单分子荧光显微镜的检测方法与力显微镜的直接机械表征结合,发现微管蛋白异构体(微管蛋白的不同变体)可作为力感受元件,调控微管腔内酶与晶格内表面底物相互作用的可达性。相关成果发表于《自然物理学》(Nature Physics),论文题为《秀丽隐杆线虫的微管蛋白异构体利用晶格的机械敏感性调控微管腔内可达性》。
为进一步解释微管蛋白异构体在腔内可达性调控中的作用机制,林元团队开发了微管三维计算模型。模拟结果显示,特定微管蛋白异构体较弱的侧向相互作用可使微管在受压时可逆形成原纤维间隙。研究团队表示,实验验证表明,这些瞬时出现的间隙尺寸足以允许腔内结合蛋白进入。
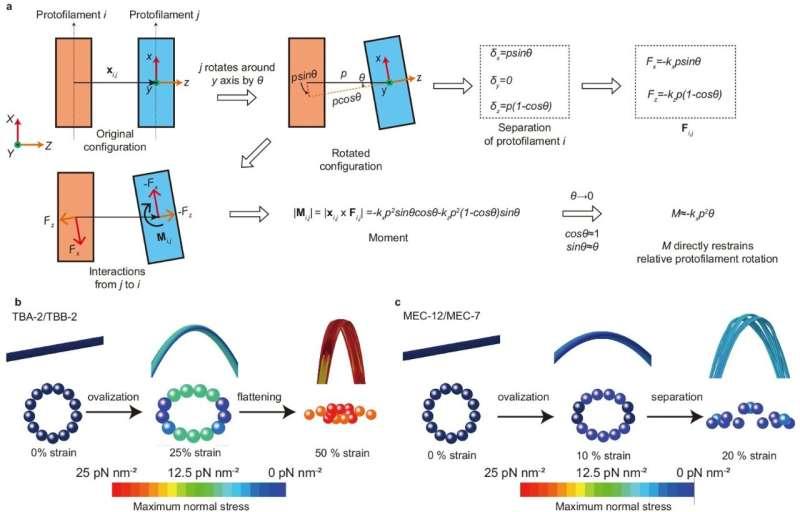
研究团队综合认为,微管蛋白异构体可通过改变原纤维间侧向相互作用强度,进而借助可逆的原纤维分离(即晶格“呼吸”)调控腔内可达性。这一机制提示,微管的机械可塑性可由其组成的微管蛋白异构体调节,从而对热诱导或应力诱导的机械变形产生不同响应。
林元与戴杰夫表示,相关发现除推进对细胞机械转导现象的理解外,也可能为未来新型主动生物材料的开发提供关键线索。
发表评论
登录后才可评论。
去登录











