理化学研究所(理研)研究人员在一项持续15年的研究中,鉴定出一种对酵母细胞内脂质连接糖链调控至关重要的酶,并据此提出糖供体水平的新的调控机制。相关成果已发表在《细胞生物学杂志》。
多烯醇连接寡糖(DLOs)是N-糖基化过程的主要糖供体。在N-糖基化中,寡糖被转移到蛋白质的天冬氨酸残基上,从而影响蛋白质的稳定性与功能。理研糖代谢生物化学实验室的铃木忠志表示,N-糖基化是一种高度保守的修饰,存在于真核生物、细菌和古细菌三大生命域。
研究人员指出,N-糖基化过程一旦发生紊乱,可能引发人类严重健康问题,包括先天性糖基化障碍(CDGs)等罕见遗传疾病,这类疾病可累及人体多个系统。
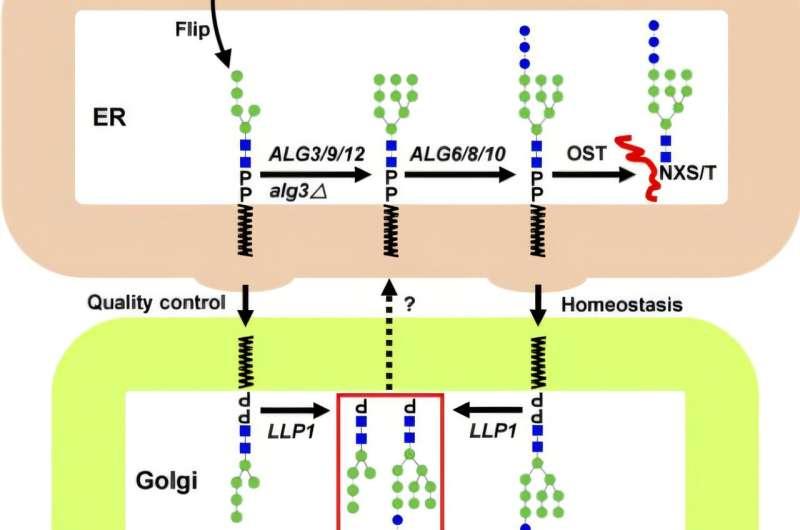
在此之前,学界已识别出参与DLO生物合成的多种基因与酶,但对DLO如何被降解了解有限。既往证据提示,DLO中间体可被分解为磷酸化寡糖(POSs),但负责释放POSs的DLO焦磷酸酶对应的编码基因一直未能确定。
铃木团队在长期探索后,最终锁定并纯化出这一关键酶,并将其编码基因命名为LLP1(脂质连接寡糖焦磷酸酶)。铃木特别提到,其博士后研究员李胜涛完成了该酶的纯化工作。研究显示,Llp1定位于高尔基体膜上;高尔基体在细胞内承担对蛋白质和脂质进行分拣并引导其到达最终位置的功能。
研究团队进一步证明,Llp1可靶向未成熟、异常以及过剩的DLO,将其分解为POSs和多烯醇磷酸(Dol-P)。其中,Dol-P可作为合成新DLO的前体。研究人员据此认为,Llp1通过调节DLO水平参与DLO的质量控制与稳态维持。铃木表示,Llp1不仅参与DLO降解,也促进新DLO及相关化合物的合成。
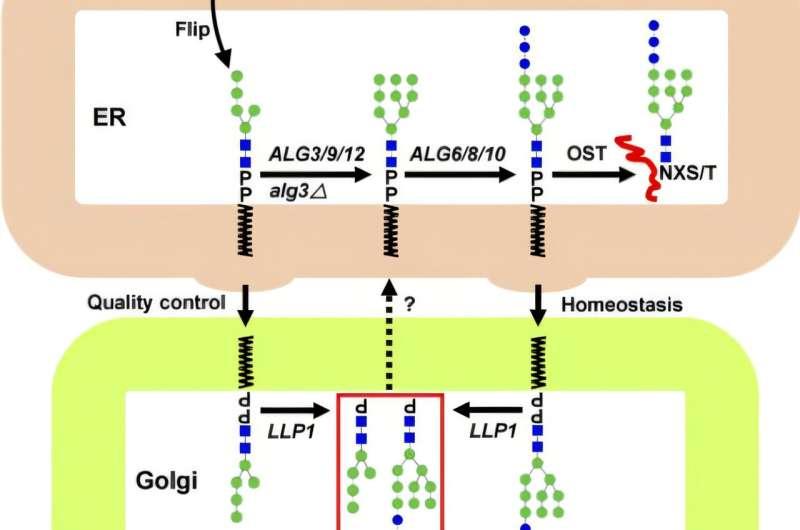
对Llp1蛋白序列的分析还显示,该酶属于VanZ样膜蛋白家族。VanZ基因存在于对抗生素万古霉素耐药的细菌中,但其功能长期未明。铃木称,团队此前并未预料到这一关联。
目前,研究团队正着手鉴定哺乳动物中与Llp1对应的基因,以期进一步揭示部分先天性糖基化障碍(CDGs)的分子机制。











