理化学研究所(理研)研究人员报告称,他们解析了一种RNA解旋酶通过选择性识别信使RNA(mRNA)特定片段来调控基因表达的分子机制。研究团队表示,该发现或可为后续合理设计调节该酶活性的药物提供依据。相关论文已发表在《自然通讯》(Nature Communications)。
研究人员指出,与具有双链螺旋结构、相对易于识别的DNA不同,由DNA转录产生的mRNA并非简单的线性带状分子,而会形成多种三维结构,这些结构会影响其被翻译成蛋白质的过程。
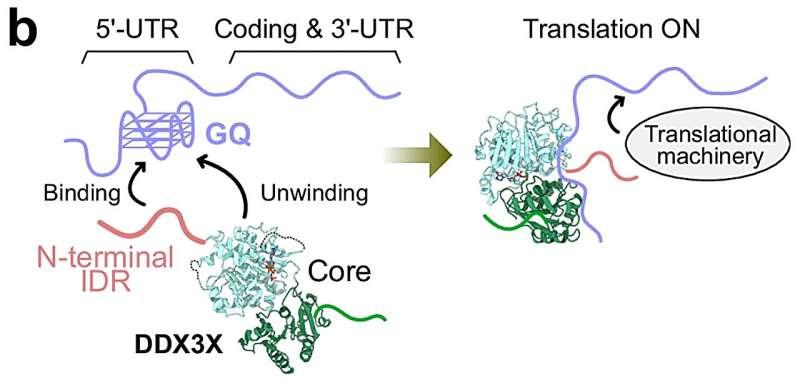
在细胞内,一类被称为RNA解旋酶的酶能够改变RNA结构。其中,DEAD-box RNA解旋酶可将RNA“拉直”,使其呈单链状态。DEAD-box RNA解旋酶家族成员DDX3X被认为只与RNA的部分片段发生相互作用,从而影响基因表达,但其特异性来源此前在分子层面仍不清楚。
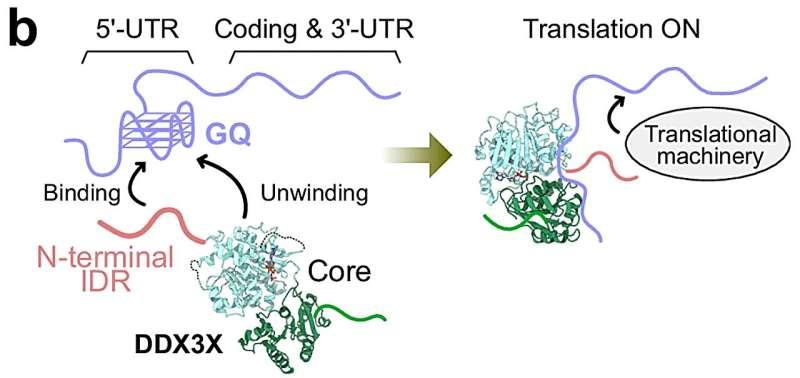
理研综合医学科学中心(IMS)的丰山裕树表示,DDX3X已知参与调控mRNA向蛋白质的翻译,且DDX3X功能异常与癌症和神经系统疾病密切相关,因此阐明其分子机制具有潜在的医学意义。
在最新研究中,丰山裕树与IMS的岛田一夫、东京大学的竹内航合作,采用溶液核磁共振(NMR)光谱技术,确定了DDX3X选择性识别mRNA特定片段的分子机制。研究团队称,出乎意料的是,DDX3X的一个天然无序区在这种选择性识别中发挥了关键作用。
岛田一夫表示,由于天然无序区缺乏明确结构,团队此前并未预期该区域会参与对RNA结构基序的特异性识别;通常此类精确的分子相互作用被认为由结构稳定的蛋白质区域介导,并常以“锁钥模型”描述。
研究人员认为,这一结果为理解其他含天然无序区蛋白质的功能提供了启示,并凸显溶液NMR在分析此类蛋白结构与相互作用中的作用。丰山裕树称,该发现强调天然无序区在细胞功能精细调控中的重要性。
团队还表示,下一步将继续研究DDX3X天然无序区的其他特征,包括其如何决定亚细胞定位。岛田一夫指出,这可能揭示该蛋白调控翻译过程的另一层机制。












