单克隆抗体已被广泛用于癌症、自身免疫疾病等多类疾病治疗,其安全性与有效性依赖于分子正确的三维构象维持,即高阶结构(HOS)的稳定。
不过,如何识别抗体中细微的结构变化仍是分析难点。圆二色谱、量热法等传统手段可提供整体层面的信息,但通常难以达到残基级分辨率。
核磁共振(NMR)光谱学能够在溶液条件下以原子分辨率观察蛋白质结构与动力学。近年来,NMR指纹图谱方法被用于评估治疗性抗体的高阶结构,但相关应用多侧重于整体光谱差异的比较,较少给出可直接解释的位点信息。
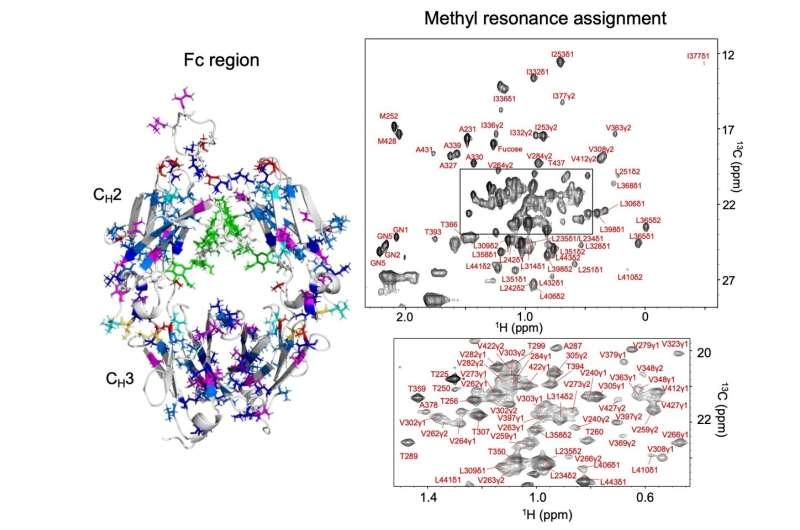
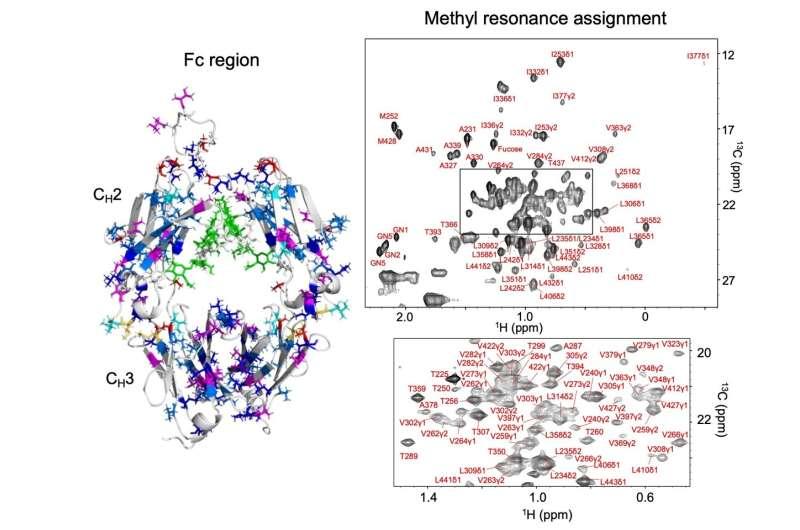
据《美国化学会杂志》发表的一项研究,生命与生命系统探索研究中心(ExCELLS)及其合作机构研究人员建立了人IgG1抗体Fc区甲基信号的位点特异性归属。研究团队结合氨基酸选择性同位素标记、诱变以及多维NMR实验,完成了Fc结构域内多类残基甲基共振信号的归属,涉及丙氨酸、异亮氨酸、亮氨酸、蛋氨酸、苏氨酸和缬氨酸等。
研究人员表示,上述归属使这些甲基信号可作为抗体结构的残基特异性探针。值得注意的是,即便在自然同位素丰度的抗体样品中也能检测到相同信号,意味着相关结构分析不必依赖同位素标记。
在应用层面,研究团队利用这些探针观察到与Fc区糖基化模式相关的结构差异,包括核心岩藻糖基化与末端半乳糖基化变化;这两类糖基特征已被认为会影响抗体效应功能。研究还指出,部分甲基信号来自抗体的高度动态区域,例如铰链区以及受体结合界面残基,这些信号可作为局部结构柔性的敏感指示,帮助识别与分子功能相关的关键区域。
研究人员认为,由于该方法可直接分析未标记抗体,为监测治疗性抗体结构完整性及细微分子变化提供了新的路径,并可用于生物制药质量控制以及生物类似药开发中的结构可比性评估。
ExCELLS的加藤浩一表示,治疗性抗体结构复杂,即使微小结构变化也可能影响其生物活性;研究显示,基于甲基的NMR信号在未标记抗体中同样可作为有力的结构探针,为抗体药物残基级结构评估提供了实用途径。
研究团队还提到,该工作与其在《分析化学》发表的相关论文形成补充。在后者中,研究人员开发了集成NMR与液相色谱-质谱(LC–MS)的方法,以残基特异性与立体化学分辨率表征IgG1 Fc区的蛋氨酸氧化。相关结果显示,保守Fc残基Met252与Met428的氧化可形成不同的R-与S-亚砜形式,并引发局部结构扰动,从而为氧化修饰影响抗体稳定性与功能提供机制性线索。
研究人员表示,两项研究共同构建了用于评估治疗性抗体高阶结构特征及化学修饰的分析框架。











