先天免疫系统依靠模式识别受体(PRRs)识别细菌或病毒入侵者的特定分子成分,并通过信号传导促使干扰素产生,从而引导免疫细胞应答。不过,相关信号如何在细胞内被精确传递,长期以来仍缺乏清晰机制描述。
科隆大学Eva Rieser博士与Henning Walczak教授领导的国际研究团队在一项新研究中表示,酶ANKIB1是先天免疫信号传导过程中的关键因子。研究显示,ANKIB1可催化一种高度特异性的分子修饰——K11-泛素化,该修饰可作为对接平台,组装启动I型和III型干扰素的机制。I型和III型干扰素被研究团队描述为人体前线的抗病毒信使。
上述研究以《赖氨酸11-泛素化驱动cGAS–STING及Toll样受体3和4诱导I型/III型干扰素》为题,发表在《自然细胞生物学》杂志。
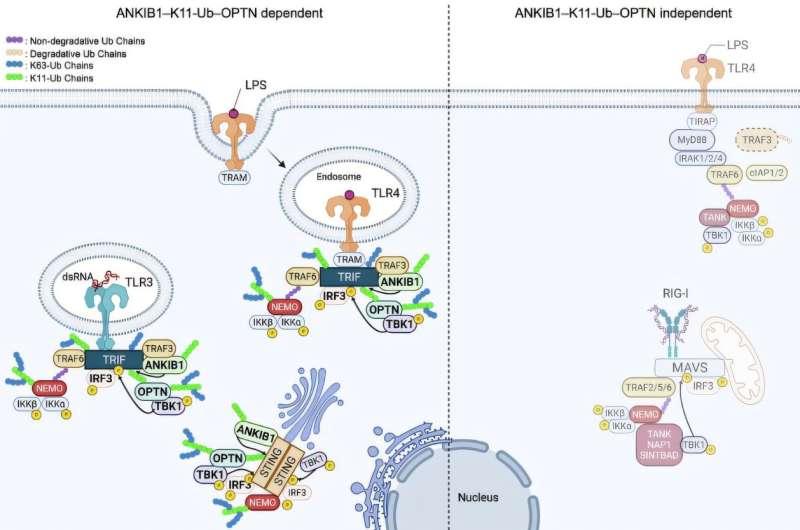
Walczak表示,研究结果表明ANKIB1不仅决定免疫细胞“警报”何时被触发,也影响该唤醒反应的强度。Rieser则指出,此前在泛素信号代码中仅已知K63和M1两种泛素链类型;此次研究将K11-泛素链类型纳入先天免疫信号传导框架,为解读细胞信号的泛素代码提供了新的线索。
研究团队通过细胞培养和动物模型实验确认,新发现的信号轴——ANKIB1–K11‑泛素–OPTN–TBK1–IRF3——对免疫系统识别病毒感染并发出警示至关重要。研究还发现,ANKIB1对抵抗单纯疱疹病毒I型感染必不可少。缺失ANKIB1的小鼠无法产生足够干扰素以警示免疫系统对抗感染,导致这种通常相对无害的病毒在实验中引发致死结果。
研究同时指出,干扰素过量会引发一系列严重炎症性疾病。在一种干扰素病的体内模型中,缺失ANKIB1的小鼠在本应致命的炎症中存活。研究团队据此认为,ANKIB1在生理必需的干扰素反应与病理性干扰素反应中均具有关键作用。
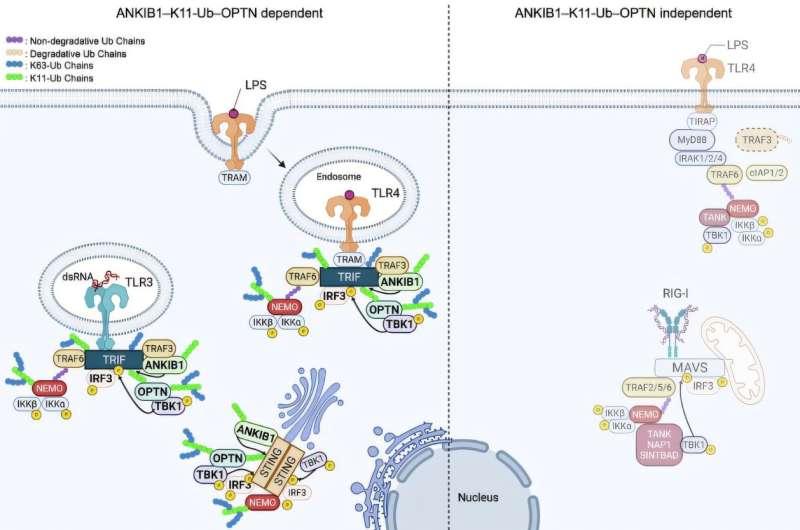
与肿瘤免疫相关的信号通路线索
该研究合作者、西班牙萨拉戈萨大学、阿拉贡健康研究所及CIBERINFEC的Julian Pardo教授表示,尽管研究基于基础生物化学与免疫学,但相关信号级联反应处于肿瘤与免疫细胞“对话”的核心。
研究文本提到,许多肿瘤会利用先天免疫通路的慢性激活,尤其是由cGAS–STING以及不同Toll样受体(TLR)触发的通路,从而在肿瘤微环境中造成慢性炎症,并抑制或阻止对癌症的有效免疫攻击。研究团队认为,明确ANKIB1及其产生的K11-泛素在这些免疫受体诱导干扰素中的决定性作用,为理解癌细胞如何调节相关通路提供了新视角。
炎症性神经疾病研究的新切入点
研究还提到,大脑中先天免疫传感器的慢性、低度激活被视为阿尔茨海默病和帕金森病等神经退行性疾病的共同特征之一,干扰素信号已被证明参与神经炎症和神经元丧失。研究团队表示,将ANKIB1界定为这些干扰素通路的关键酶,有助于为解析大脑炎症信号的同步机制提供框架,并阐明异常干扰素产生与神经退行性变之间的关联。
Walczak称,对机制的解析精确到泛素链类型及其生成酶,使复杂免疫级联反应在机制层面更具体,也更便于作为潜在可干预环节被研究。研究文本同时提出,在不全面抑制免疫系统的情况下,围绕ANKIB1催化活性或其稳定性的调节,可能为干扰素驱动的自身炎症和免疫疾病提供新的研究方向;在需要更强抗病毒或抗肿瘤免疫的情境下,短暂增强ANKIB1活性或稳定K11-泛素也被提及为可探讨的路径。











