科研团队在小鼠模型中验证阿尔茨海默病可逆性原理
由凯斯西储大学、大学医院及路易斯·斯托克斯克利夫兰退伍军人医疗中心牵头的科研团队报告称,在多种阿尔茨海默病(AD)小鼠模型中,通过药物干预恢复大脑中烟酰胺腺嘌呤二核苷酸(NAD+)的稳态,可在疾病晚期实现病理和功能层面的显著恢复。相关成果已发表于《Cell Reports Medicine》杂志。
研究人员表示,这一结果为晚期阿尔茨海默病治疗具有可逆性提供了原理性证据。
NAD+稳态被指为疾病关键驱动因素
研究团队在分析人类阿尔茨海默病脑组织及多种临床前小鼠模型后发现,大脑无法维持细胞能量核心分子NAD+的正常水平,与阿尔茨海默病的发生和进展密切相关。论文指出,阿尔茨海默病严重程度与NAD+稳态失调呈相关关系。
NAD+稳态被认为是细胞应对氧化应激、DNA损伤、神经炎症、血脑屏障退化、海马神经发生受损、突触可塑性缺陷及神经退行性变等多种病理过程的核心环节。研究团队在阿尔茨海默病患者大脑中观察到NAD+水平明显下降,并在阿尔茨海默病小鼠模型中发现了类似变化。
小鼠模型显示病理与认知缺陷可被逆转
阿尔茨海默病被认为是人类特有疾病,但可通过携带致病突变的小鼠模型进行研究。本次研究采用了两类基因工程小鼠:一类携带多个人类淀粉样蛋白处理相关突变,另一类携带人类tau蛋白突变。
两种模型小鼠均出现与阿尔茨海默病相似的大脑病理特征,包括血脑屏障退化、轴突退化、神经炎症、海马神经发生受损、突触传递减少以及广泛的氧化损伤积累,并表现出严重的认知障碍。
在确认人类和小鼠阿尔茨海默病大脑中NAD+水平显著下降后,研究人员进一步测试:在疾病发生前预防大脑NAD+失衡,是否可以阻止疾病发展;以及在疾病已显著进展后恢复NAD+平衡,是否可以逆转病程。
团队在此前关于严重、长期创伤性脑损伤的研究基础上,选用一种已被充分表征的药理剂P7C3-A20,以恢复大脑NAD+稳态。结果显示,维持NAD+平衡不仅可防止小鼠发展出阿尔茨海默病样病理,在疾病晚期开始给药也能促使大脑修复由致病基因突变驱动的主要病理改变。
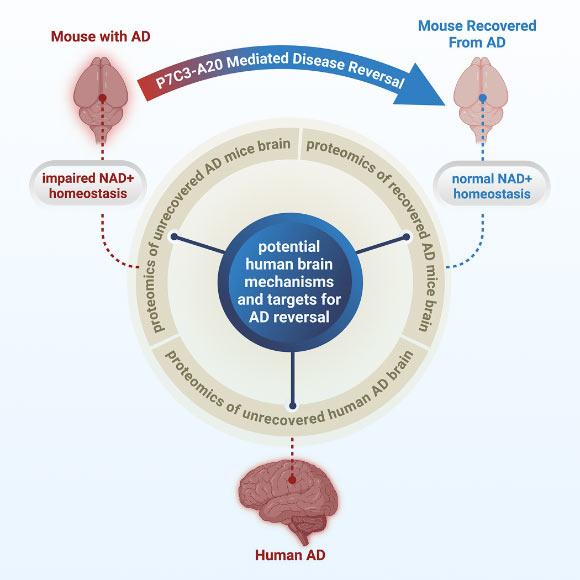
研究报告称,两种小鼠模型在治疗后均实现了认知功能的完全恢复。同时,血液中磷酸化tau 217水平恢复至正常范围。磷酸化tau 217是近期获批用于人类阿尔茨海默病的临床生物标志物,该结果被研究团队视为疾病逆转的客观指标,并被认为为未来阿尔茨海默病恢复相关临床试验提供了潜在的监测工具。
研究者:大脑在特定条件下具备自我修复能力
研究团队指出,部分携带常染色体显性阿尔茨海默病突变的人群在临床发病前可长期保持无症状状态,另有部分被归类为“具有阿尔茨海默神经病理但无痴呆”的个体,即便脑内已积累大量淀粉样斑块,认知功能仍然保持完整。这些现象被研究者视为大脑存在内在弹性机制的证据,可能延缓或抵消疾病进展。
凯斯西储大学的Andrew Pieper教授表示,在两种由不同遗传因素驱动的阿尔茨海默病小鼠模型中,恢复大脑能量平衡均带来了病理和功能层面的恢复,这强化了一个新观点:当大脑NAD+平衡得以恢复时,晚期阿尔茨海默病患者可能存在恢复的可能性。
Pieper教授称,这些结果促使研究人员、临床医生和患者重新思考未来阿尔茨海默病治疗的潜在方向。他指出,研究显示,在特定条件下,受损大脑可以通过自身机制进行修复并恢复功能。
凯斯西储大学及大学医院研究员Kalyani Chaubey博士表示,团队通过药物手段在动物模型中实现了这一目标,并在人体阿尔茨海默病脑组织中鉴定出一批可能与逆转疾病能力相关的候选蛋白,为后续研究提供了线索。
药理策略区别于市售NAD+前体
研究团队提到,目前市面上可获得的NAD+前体在动物模型中已被证实会将细胞NAD+水平提升至危险的高值,从而促进肿瘤发生。而本研究采用的P7C3-A20则通过支持细胞在极度压力条件下维持适当的NAD+平衡,并不将NAD+推升至超生理水平。
Pieper教授表示,这一区别在考虑患者治疗策略时具有重要意义。他认为,恢复大脑能量平衡的治疗路径可能为阿尔茨海默病恢复提供一种新的思路。
论文信息
该研究以题为《小鼠晚期阿尔茨海默病的药理逆转及人类大脑潜在治疗节点的鉴定》(Pharmacologic reversal of late-stage Alzheimer’s disease in mice and identification of potential therapeutic nodes in the human brain)发表于《Cell Reports Medicine》,在线发表日期为2025年12月22日,论文第一作者为Kalyani Chaubey,DOI为10.1016/j.xcrm.2025.102535。











