尽管DNA在细胞核内被紧密包装并受到多重保护,但在正常代谢过程中以及辐射、化学物质等外部压力作用下,DNA仍会持续遭受损伤。细胞依赖一套复杂的修复机制网络维持基因组稳定;当修复系统受损,DNA损伤可能累积并影响细胞功能,进而与癌症、衰老及退行性疾病相关。
在多种DNA损伤类型中,DNA-蛋白交联(DNA-protein crosslinks,DPCs)被认为对基因组完整性威胁较大。该损伤表现为蛋白质异常附着在DNA上,可能由饮酒、接触甲醛或其他醛类物质引发,也可能源于参与DNA复制与修复的酶发生错误。由于DPCs可阻滞DNA复制并在细胞分裂过程中造成严重差错,其清除对维持细胞正常增殖至关重要。
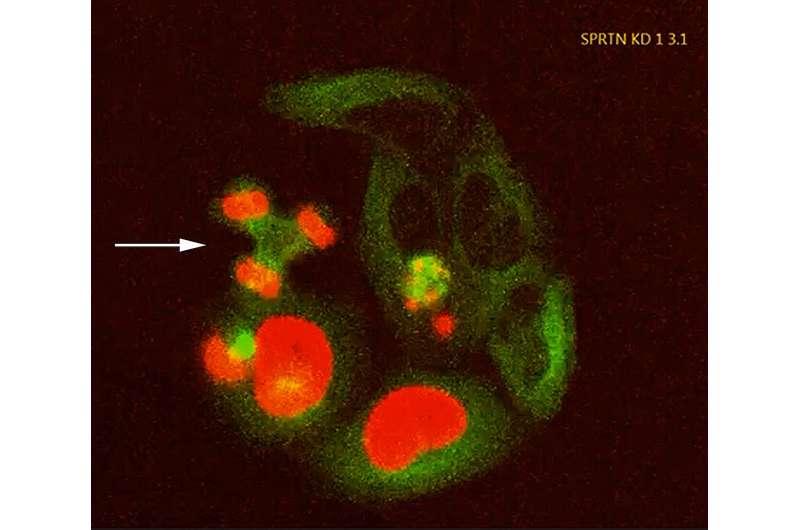
研究显示,酶SPRTN可通过切割方式去除DPCs。若SPRTN因突变等原因功能失常,个体可能在青少年时期出现骨骼畸形并易患肝癌,这一罕见遗传病被称为Ruijs-Aalfs综合征。此前,该综合征的具体致病机制仍不清楚,且缺乏特异性治疗手段。
核内DNA外泄触发免疫信号
由歌德大学生物化学研究所II的Ivan Ðikić教授领导的研究团队在细胞培养实验与基因改造小鼠模型中发现,功能性SPRTN的缺失不仅会导致细胞核内受损DNA积累,还会使核内DNA泄漏至细胞质。研究成果发表于《Science》。
研究团队指出,细胞质中的DNA通常被细胞视为危险信号,因为这类DNA往往与入侵的病毒或细菌、或恶性转化相关。细胞因此可通过cGAS-STING信号通路启动防御反应,并释放信使物质招募免疫细胞,进而形成慢性炎症。
慢性炎症与早衰表型相关
研究人员观察到,在相关小鼠模型中,慢性炎症反应在胚胎阶段尤为明显,并可持续至成年,表现较突出的器官包括肺和肝脏。研究结果显示,小鼠可能出现早逝,或呈现与Ruijs-Aalfs综合征患者相似的早衰迹象。研究还发现,阻断相关免疫反应可缓解多项症状。
Ðikić表示,未被修复的DNA-蛋白交联可能带来更广泛的系统性影响:不仅破坏基因组稳定性,还可驱动慢性炎症,从而对寿命产生显著影响。
为潜在靶向治疗提供线索
研究团队认为,该发现除有助于解释Ruijs-Aalfs综合征外,也可能为其他与DNA-蛋白交联相关的罕见遗传病研究提供基础。研究人员表示,通过解析这些罕见疾病的机制,可进一步揭示DNA损伤、炎症反应与机体寿命之间的联系,并为理解衰老生物学提供新的线索。











