科学家近日报告称,已在分子层面识别出支撑蜘蛛丝兼具高强度与高柔韧性的关键相互作用,为开发面向航空、保护装备与医疗等领域的仿生纤维材料提供了可借鉴的设计思路。
伦敦国王学院与圣地亚哥州立大学(SDSU)的研究人员在《美国国家科学院院刊》(Proceedings of the National Academy of Sciences)发表上述成果。研究团队表示,这些发现有望形成可用于指导新一代高性能、可持续纤维研发的通用设计原则。
研究首次展示了蜘蛛丝蛋白内部氨基酸之间如何发生协同作用,并在纤维形成过程中表现为类似“分子粘合剂”的效应。伦敦国王学院计算材料科学教授克里斯·洛伦兹(Chris Lorenz)称,基于这些天然机制设计的纤维,潜在应用包括轻质防护服、飞机部件、生物降解医疗植入物以及软体机器人等。
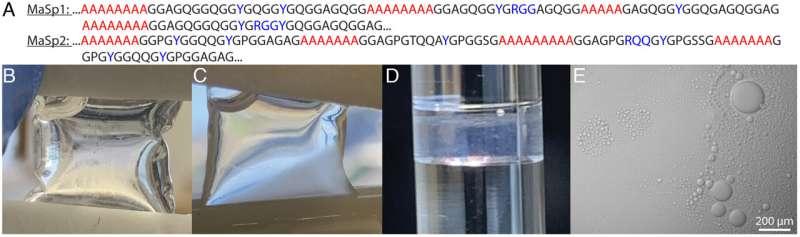
蜘蛛拖线丝以其突出的力学性能受到关注:按重量计算,其强度超过钢铁,韧性也高于用于防弹衣的凯夫拉材料。拖线丝由蜘蛛丝腺产生,相关蛋白以浓缩液体形式储存为“丝液”,随后被纺丝形成固态纤维。尽管此前已知丝蛋白会先凝聚成类似液滴的形态并被挤出成纤维,但将这一过程与最终纤维结构直接关联的分子机制一直未被清晰解释。
为厘清这一环节,由化学家、生物物理学家与工程师组成的跨学科团队结合分子动力学模拟、AlphaFold3 结构建模与核磁共振光谱等计算与实验手段,指出精氨酸与酪氨酸之间的相互作用可触发丝蛋白的初始聚集。研究进一步显示,这类相互作用在纤维形成过程中持续存在,并参与构建赋予蜘蛛丝卓越机械性能的复杂纳米结构。
洛伦兹表示,该研究从原子尺度解释了无序蛋白如何组装为高度有序、且具高性能的结构。
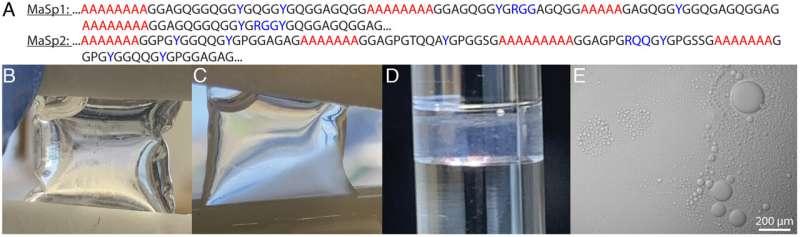
SDSU 物理与分析化学教授格雷戈里·霍兰德(Gregory Holland)指出,研究中一个出人意料的发现是蜘蛛丝形成过程所涉及的化学机制复杂程度。“丝通常被认为是一种非常简单的天然纤维,但我们的结果显示,它依赖于高度复杂的分子机制,”霍兰德说,并补充称,研究识别到的相互作用类型也可见于神经递质受体与激素信号传导过程。
霍兰德同时表示,这一发现可能对人类健康相关研究具有延伸意义。他提到,丝蛋白经历相分离并形成富含 β 折叠结构的过程,与阿尔茨海默病等神经退行性疾病中观察到的机制存在相似之处;研究蜘蛛丝可提供一个“清晰且经过进化优化的系统”,以帮助理解如何调控相分离与 β 折叠结构的形成。











