G蛋白偶联受体(GPCR)是人体内数量最多的一类细胞表面蛋白,可识别激素、神经递质及药物,并参与调控多种生理过程。该类受体也是目前市场上超过30%药物的作用靶点。组胺H1受体(H1R)作为GPCR的一个亚型,与过敏反应、炎症、血管通透性、气道收缩以及觉醒和认知功能等过程相关。尽管抗组胺药主要针对H1R,但疗效仍存在局限,促使研究人员从新的角度审视H1R配体的作用机制。
从亲和力走向结合热力学
近年来,药物设计的关注点不再仅限于配体与靶蛋白的亲和力或结合能,还逐步强调结合能的组成——焓与熵的贡献。研究人员认为,焓-熵补偿等概念有助于解释配体选择性与异构体特异性。不过,焓与熵等热力学参数的直接实验测量在膜蛋白体系中仍较具挑战。
在这一背景下,日本东京理科大学(TUS)生命系统工程系白石光纪教授团队对H1R的结合热力学开展系统研究。研究由博士一年级学生金子浩人及副教授安藤忠等参与,相关成果于2026年1月26日在线发表于《ACS Medicinal Chemistry Letters》。
以多塞平E/Z异构体为模型
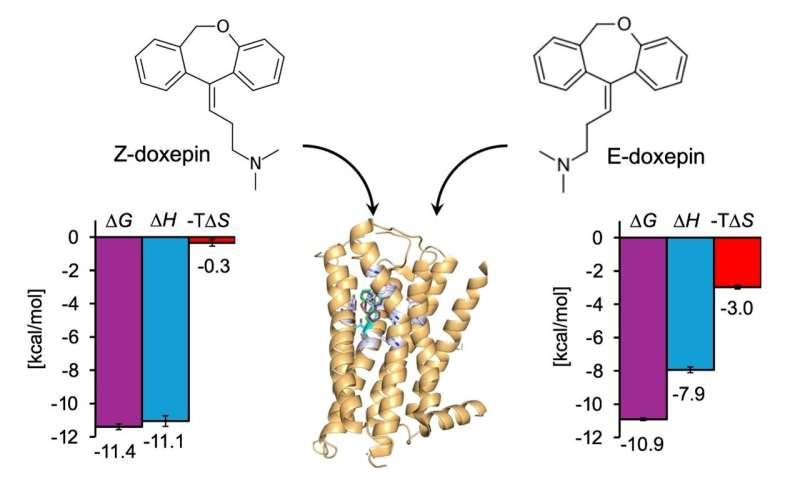
研究选取多塞平作为模型配体。多塞平是一种三环类抗抑郁药,同时也是常用的H1R抑制剂,通常以E-与Z-几何异构体混合物形式存在。既往研究显示,Z-异构体对H1R的亲和力约为E-异构体的五倍,并指出受体中的关键苏氨酸残基Thr1123.37与这种异构体依赖性选择性相关。
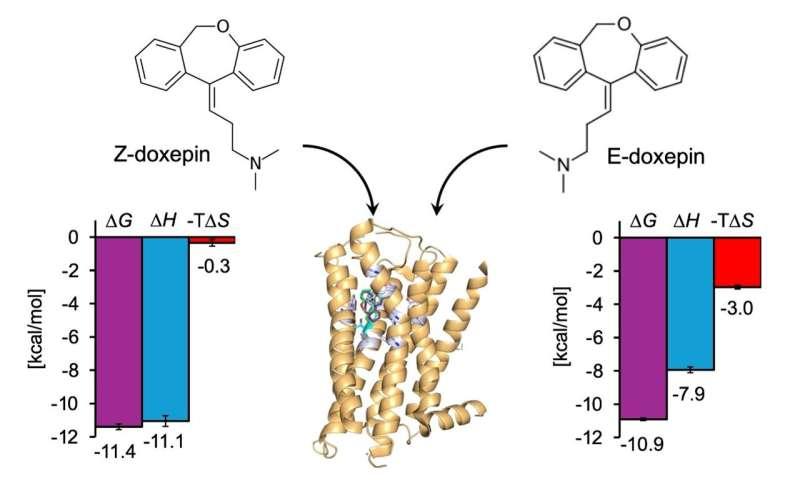
为进一步解释上述差异,研究团队利用酿酒酵母表达系统制备受体,并结合等温滴定量热法与分子动力学模拟,测量并分析多塞平E/Z异构体与H1R的结合热力学特征。
受体突变验证关键残基作用
研究人员构建并比较了两种受体:野生型H1R(H1R_WT)以及T1123.37V突变体(将Thr1123.37替换为另一种氨基酸)。随后,团队分别测试两种受体与多塞平混合物以及单独E-、Z-异构体的结合情况,以评估Thr1123.37对结合过程的影响。
实验结果显示,H1R_WT与T1123.37V突变体在总体结合能方面差异不显著,但焓与熵的贡献出现明显分化:H1R_WT的结合更偏向焓驱动,而突变体中焓贡献降低、熵贡献相对增加。
在异构体层面,Z-异构体与H1R_WT结合时表现出更大的焓增益,同时伴随更显著的熵损失,相较E-异构体差异更为突出;但在T1123.37V突变体中,这些差异不再明显。研究还观察到,Z-异构体在H1R_WT上的结合能高于E-异构体,而在突变体中两者结合能趋于相当,与既往关于亲和力差异的结论一致。
研究团队据此指出,Thr1123.37可能在配体结合过程中参与调节焓增益与熵损失之间的平衡,并且对Z-异构体的影响更为显著。
分子动力学模拟指向“构象限制”
为解释Z-异构体高亲和力的分子基础,研究人员进一步开展分子动力学模拟。模拟结果显示,Z-异构体的高亲和力结合与构象限制相关,这与实验中观察到的“高焓、低熵”特征相一致。
白石光纪表示,这些关于GPCR-配体相互作用中焓-熵权衡的机制性信息,提示在设计具备优化热力学性质的配体时,需要将构象限制与分子柔性纳入考虑。研究团队同时指出,将结合热力学分析与分子动力学模拟结合的方法,也可推广至其他GPCR及蛋白质体系,用于支持合理药物设计。
对药物研发的意义
研究认为,分子构象的细微变化可能改变焓-熵平衡,从而影响配体选择性与结合特征。团队表示,对这些热力学机制的理解有助于为后续药物设计提供框架,并为进一步探索GPCR及其他蛋白质-药物相互作用中的焓-熵关系提供参考。











