凯泽斯劳滕-兰道应用技术大学研究人员报告称,糖分解过程中的一种中间产物不仅与能量获取有关,还可能在细胞运动性调控中发挥关键作用。相关研究已发表在《自然细胞生物学》(Nature Cell Biology)上。研究团队表示,该发现有助于进一步理解胚胎发育中的细胞迁移、转移性癌细胞迁移以及伤口愈合等生物过程。
细胞粘附结构与迁移的动态重塑
研究人员指出,人体由约32万亿个细胞构成。为维持组织结构,多数细胞需要通过特定结构与周围环境牢固连接,其中包括焦点粘附等锚定点。焦点粘附由蛋白质复合体组成,一端与细胞外分子结合,另一端连接细胞骨架系统。
在细胞迁移过程中,例如伤口修复或胚胎发育阶段,细胞骨架与焦点粘附需要持续进行组装与拆解的动态循环。研究团队提到,如果这一重塑过程出现紊乱,可能与肿瘤细胞扩散相关,而调控细胞骨架与粘附结构重塑的具体机制仍未完全明确。
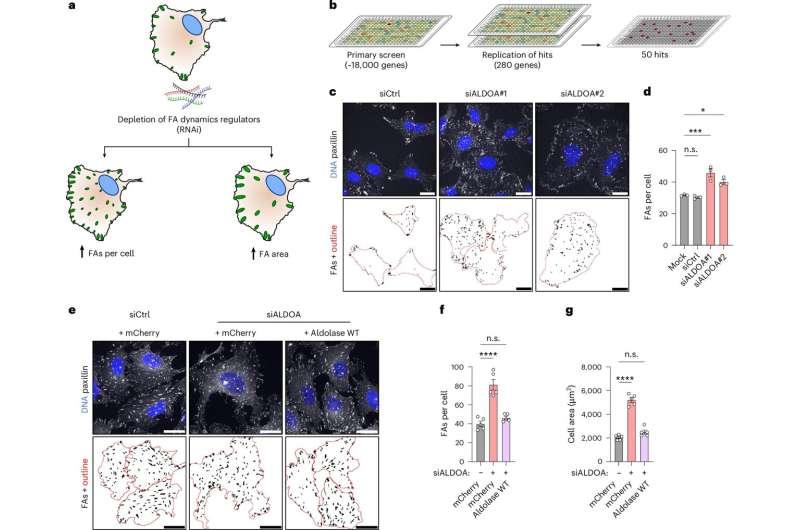
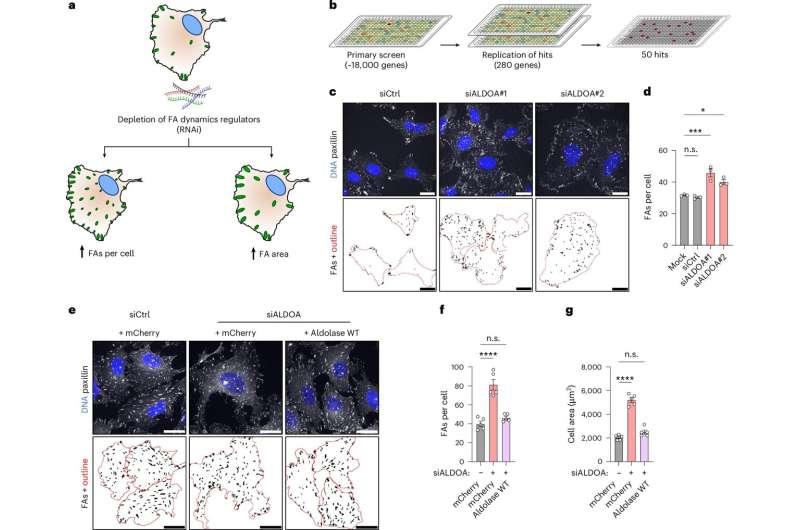
siRNA筛选覆盖约1.8万种蛋白质
该研究由坦娅·马里岑(Tanja Maritzen)教授团队牵头,并与莱布尼茨分子药理学研究所筛选与细胞成像单元合作开展。研究人员采用小干扰RNA(siRNA)抑制单个蛋白质的产生,随后通过显微观察与自动图像分析评估细胞粘附结构的数量与大小变化。
马里岑表示,团队通过对细胞粘附结构进行染色并在显微镜下观察,再利用自动化图像分析判断粘附结构是否发生改变。研究共检测了人体内约18,000种不同蛋白质。结果显示,当代谢酶醛缩酶A缺失时,细胞体积增大且焦点粘附数量增加。研究还发现,在醛缩酶缺失的细胞中会积累一种特定糖分子,该分子可与特定蛋白结合,并触发与细胞运动相关的过程。
FBP被指连接能量代谢与细胞运动信号
研究第一作者伦纳特·霍夫曼(Lennart Hoffmann)称,团队识别出糖代谢中的小分子果糖1,6-二磷酸(fructose 1,6-bisphosphate,简称FBP)除作为糖转化为能量的中间产物外,还可作为信号分子参与细胞骨架与粘附结构的重塑。
研究进一步指出,FBP可促使细胞骨架重塑相关的激活因子Rac1蛋白从非活性状态转为活化状态。研究人员描述,活化的Rac1会推动细胞前端形成新的细胞骨架元素,带动细胞膜向前移动,并通过形成新的粘附点实现锚定。
马里岑表示,学界长期怀疑细胞能量代谢会影响细胞骨架重塑与粘附结构形成。她指出,在细胞进行耗能的骨架重塑之前获得能量状态反馈具有合理性。
研究称或有助理解多类生物过程
研究团队认为,该机制对细胞粘附与迁移研究具有意义。马里岑表示,免疫细胞以及转移性癌细胞的迁移可能受到该机制影响。
研究人员同时提到,细胞骨架还参与新血管形成与胰岛素分泌等过程,因此相关发现也可为上述领域研究提供参考。











