人体内每秒有数百万个细胞完成分裂。在这一过程中,细胞会在约一小时内复制DNA,并在染色体周围组装出由蛋白质纤维构成的纺锤体结构。纺锤体将多条纤维从位于细胞中央的染色体延伸至细胞边缘,并在分裂阶段施加强大拉力,将染色体分开。
纺锤体如何在承受巨大机械应力的同时避免自身受损,长期以来缺乏直接证据。旧金山加州大学(UCSF)的研究人员最新报告称,纺锤体在拉扯DNA的过程中能够进行自我修复,并在工作中替换较脆弱的连接,从而持续增强结构强度,确保DNA被准确分成两份。研究人员指出,细胞中多出一个染色体可能与癌症或出生缺陷相关。
上述研究已发表在《Current Biology》杂志。
通过微针直接测试纺锤体纤维强度
论文通讯作者、旧金山加州大学生物工程与治疗科学以及生物化学与生物物理学教授Sophie Dumont表示,纺锤体能够产生巨大力量,因此必须具备很高的结构强度,但对其强度进行直接测量并不容易;相关实验为理解这一分子机器为何可靠提供了线索。
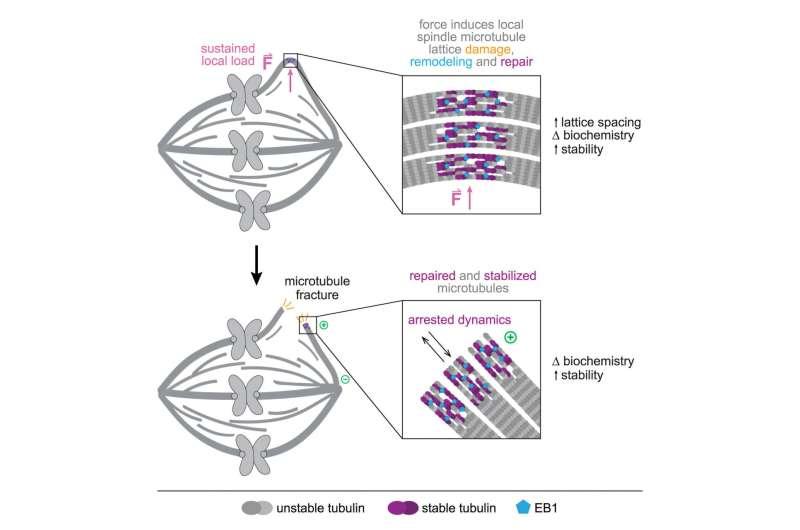
为观察纺锤体纤维在压力下的形变与断裂方式,第一作者、旧金山加州大学研究生Caleb Rux使用微针进行拉伸测试。研究团队介绍,微针由玻璃制成,拉伸后比人类头发更细,且末端经过处理以保持光滑,避免刺破细胞导致细胞死亡。
在显微镜下,Rux选择纺锤体从细胞一端延伸至另一端、染色体位于中央并即将分裂的拉长细胞进行操作。他通过类似Etch-a-Sketch的X-Y旋钮远程定位微针至纺锤体纤维上方,再用第三个旋钮降低针头并释放控制。随后,研究人员启动经过精密校准的电机,使针头逐步拉扯纤维直至其断裂。
断裂位置与纤维行为呈现“自我强化”特征
Rux表示,团队原本预期纺锤体纤维会在两端断裂,但实验中纤维却在微针施力的位置发生断裂。
研究人员还观察到,纤维断裂后的末端仍能保持形状,没有出现回缩或解体。这一现象与团队此前使用激光作用于纤维时观察到的解体结果不同。
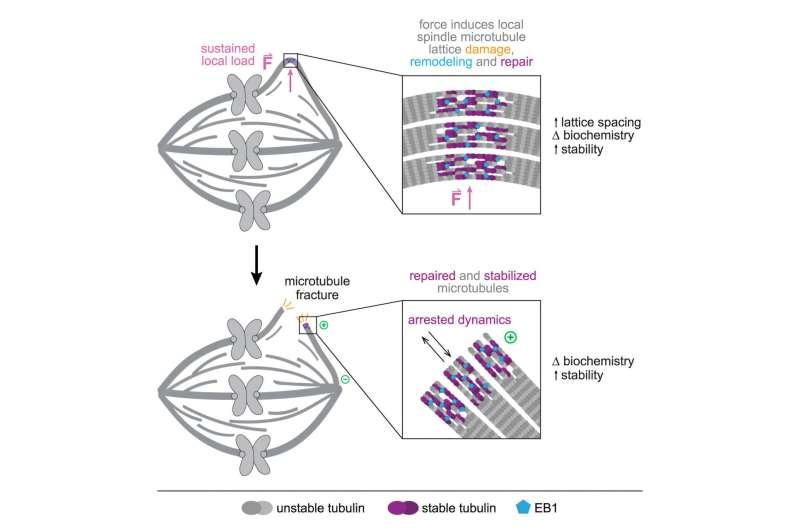
进一步测试显示,当纺锤体最初被微针拉伸时,部分蛋白质连接会先行断开,但纤维会迅速以周围漂浮的更强连接进行替换,从而抵御持续的物理挑战。研究人员称,在最终断裂发生时,纺锤体结构相较受力前已更为坚固。
Dumont表示,这一结果提示纺锤体可能会在受力最大的区域实现自我稳定。
该研究其他作者包括Megan K. Chong、Valerie Myers和Nathan H. Cho。











