研究人员正尝试通过不同路径预防1型糖尿病。与以往主要聚焦抑制自身免疫反应的策略不同,芝加哥大学科学家在一项新研究中提出,通过增强胰岛β细胞的“自我保护”能力来维持其功能。
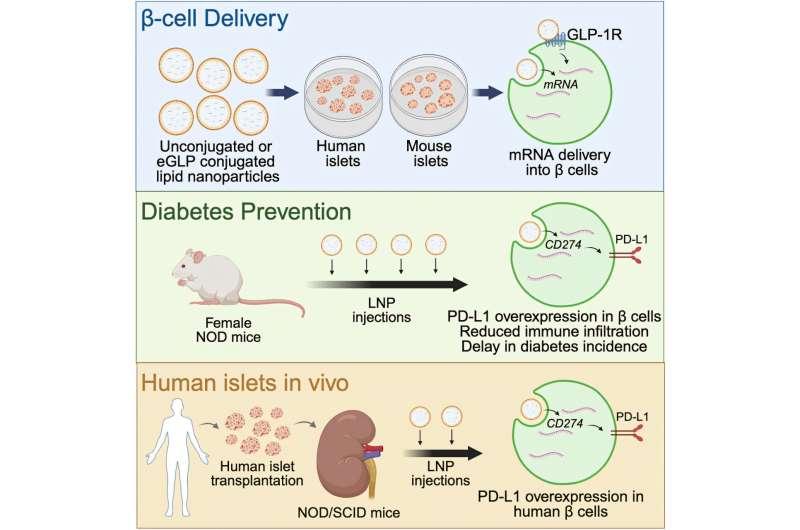
本周发表于《Cell Reports Medicine》的研究显示,团队使用由脂质构成的纳米颗粒递送mRNA分子至β细胞,促使细胞表达更多PD-L1蛋白。PD-L1是一种细胞表面蛋白,可抑制免疫反应并限制T细胞活性,从而在自身免疫、炎症或感染过程中减少对健康组织的损伤。研究人员指出,癌细胞也常借助PD-L1逃避免疫系统识别,因此相关免疫疗法通常以阻断PD-L1为目标。
论文通讯作者之一、芝加哥大学博士后学者Jacob Enriquez表示,在这项初步的治疗概念验证中,研究团队展示了可通过纳米颗粒系统递送PD-L1 mRNA,延缓小鼠1型糖尿病的进展,并在人体细胞实验中显示出潜在转化意义。
研究团队来自芝加哥大学医学教授Raghu Mirmira的实验室,并与医学教授Yun Fang以及前芝加哥大学博士后、现任天普大学的Zhengjie Zhou合作。研究人员称,团队长期从事纳米颗粒递送治疗性载荷的研究。在本项工作中,Zhou设计了一种由四种脂质组成的纳米颗粒,用于包裹mRNA分子,其技术路径与部分新冠疫苗所采用的脂质纳米颗粒递送方式相似。
Fang表示,纳米医学方法是RNA疫苗获得临床成功的关键之一;本研究提出的概念与技术进展,为通过选择性靶向胰岛素产生细胞,并进一步扩展至1型糖尿病相关的其他关键细胞类型的治疗探索提供了基础。
在靶向策略上,研究人员设计了两种纳米颗粒版本:一种在颗粒表面加入肽标签,用于靶向β细胞表面的GLP-1受体;另一种则不带肽标签。研究显示,在体外实验中,两种版本均可提升小鼠与人类β细胞中的PD-L1表达,其中带GLP-1受体靶向标签的版本在小鼠细胞中表现略优。
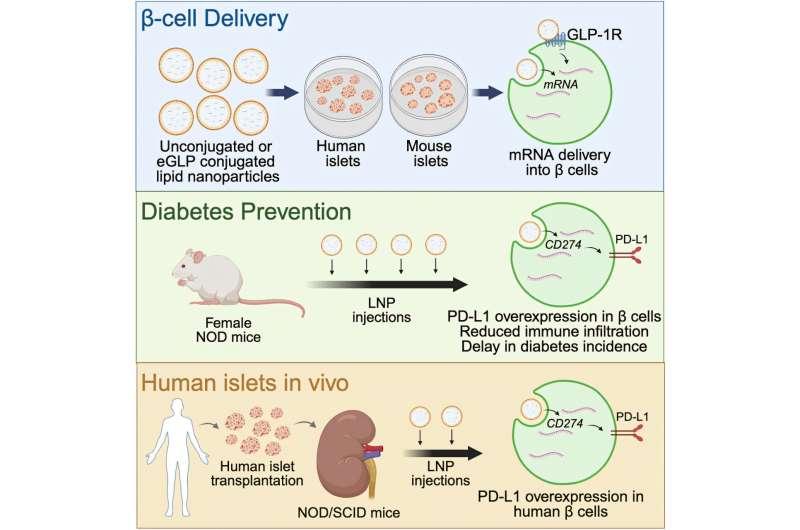
研究还在模型中验证了该递送方式的效果:在将人类胰岛细胞移植至小鼠体内后注射纳米颗粒,同样能够诱导PD-L1表达。
研究人员表示,理想情况下,这类干预应在疾病完全发作前实施,即在仍有部分β细胞保持功能时,以保护胰岛素生成能力。团队同时指出,两种纳米颗粒版本均可靶向β细胞而不影响其他细胞类型,有助于降低非预期副作用风险。研究团队还计划探索递送其他治疗分子,并通过增加更多表面肽以提升对人类β细胞受体的靶向效率。
Mirmira表示,这项工作带来新的研究方向,即利用既有知识对β细胞进行工程化改造;从工具层面看,能够在不损害其他细胞的情况下靶向特定细胞类型,具有潜在应用价值。












