莱比锡大学与德累斯顿工业大学研究人员报告称,已开发出一种可通过光脉冲选择性开启或关闭离子通道的分子“生物开关”。研究团队表示,相关分子在初步实验中可用于光刺激激活脑内特定神经细胞群体,并实现对肾上腺细胞肾上腺素释放以及小肠收缩与舒张的调控。
相关研究已发表于《Nature Chemical Biology》。
研究人员介绍,离子通道位于细胞膜上,承担对钠、钾、钙等离子定向运输的选择性门控功能,并可根据不同刺激信号在开放与关闭状态间切换,例如响应电信号、化学分子或细胞内信使。离子通道在大脑、肾上腺与消化道等多种器官系统中发挥作用。
本项工作聚焦于瞬时受体电位(TRP)家族中的TRPC4与TRPC5两种离子通道。研究团队的关键进展在于提出一种“效能开关”思路:通过设计新化合物,使其活性能够被光以可逆方式调控——在紫光照射下表现为通道激活剂,在蓝光照射下则转为通道抑制剂。
为实现上述可逆调控,研究人员将能够影响TRPC4与TRPC5通道的化合物与化学光开关结构结合,使分子在“开”与“关”两种状态间切换。两种新分子被命名为AzPico与AzHC,研究团队称其可作为分子光开关,通过定向外部光刺激控制通道活性。
研究人员进一步指出,该方法的控制方式并非仅限于简单的开关:调控效果的强弱与所用光的颜色相关,光开关在功能上更接近“调光器”,可实现对效应强度的精细设定。
鲁道夫·博姆药理与毒理学研究所所长、莱比锡大学教授迈克尔·谢弗表示,通过团队提出的“色控”方法,可在空间与时间上以高精度、并以明确定义的强度对细胞或器官功能进行刺激与调节。该研究由谢弗与德累斯顿工业大学奥利弗·索恩-塞斯霍尔德教授合作领导。
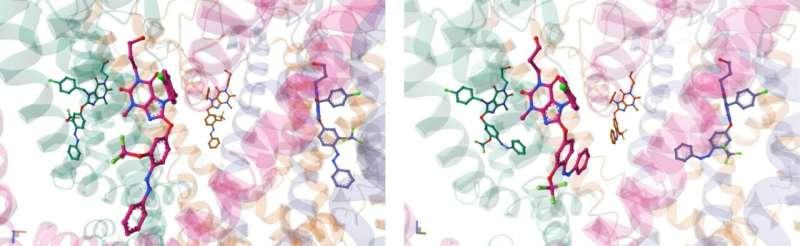
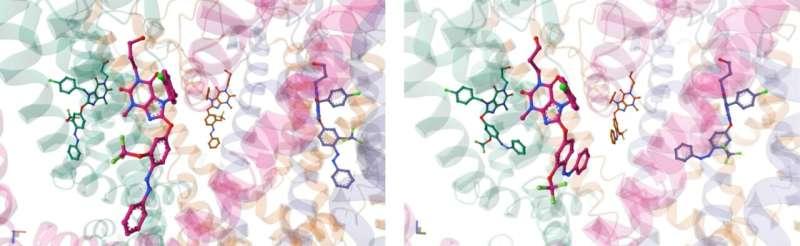
在机制层面,研究团队与利兹大学罗宾·邦教授以及多特蒙德马克斯·普朗克分子生理学研究所斯特凡·劳恩泽教授合作,利用高分辨率冷冻电子显微镜解析了两种新光开关的精确结合位点。研究人员还表示,基于基因修饰小鼠系的实验结果显示,TRPC4与TRPC5光开关具有较高的选择性与特异性。
研究团队称,后续将继续评估TRPC4与TRPC5离子通道在其他重要器官系统中的作用,并推进可被更长波长光激活的后续化合物研发,以期实现对更深层组织的可靠靶向。研究人员表示,这类光控分子有助于进一步理解复杂生理功能,并为开发具备区域性与时间性可调特征的治疗方案提供支持。
该研究在跨区域合作研究中心152框架内完成。











