杜克大学工程师近日展示一种借助微泡与超声,将较大分子抗癌药物导入肿瘤细胞并诱导其自毁的递送技术。该平台名为“超声穿孔辅助精确细胞内纳米递送”(SonoPIN)。研究团队在台式实验中观察到,采用该方法后,约50%的靶向癌细胞发生自毁,而约99%的非靶向细胞保持健康。相关研究已发表于《美国国家科学院院刊》(Proceedings of the National Academy of Sciences)。
PROTAC药物与靶点
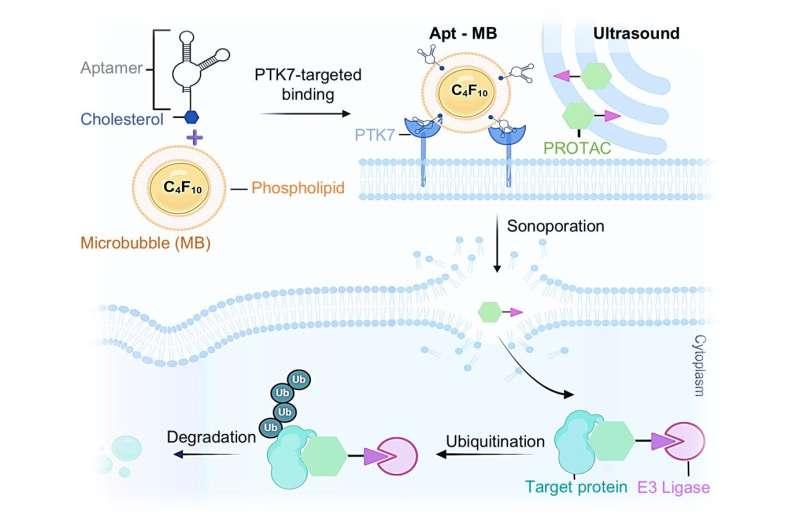
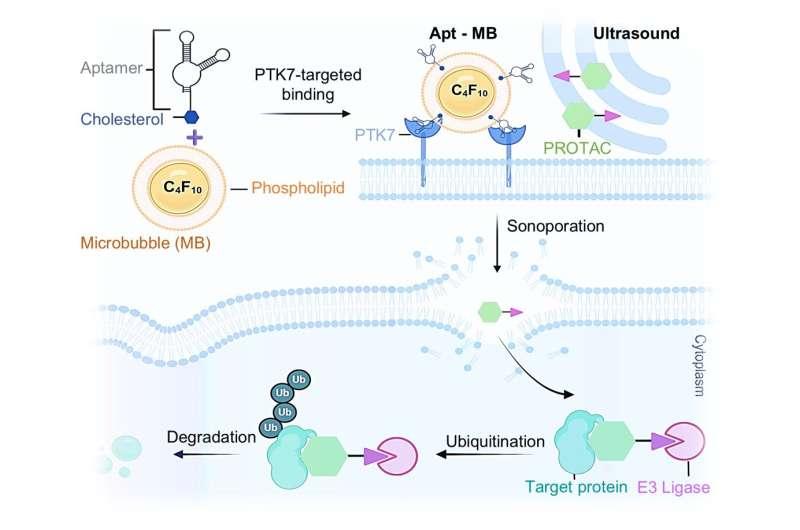
研究聚焦于一类新兴治疗药物“蛋白酶体靶向嵌合体”(proteolysis-targeting chimeras,PROTACs)。研究人员介绍,PROTACs通过结合特定靶蛋白并招募E3泛素连接酶,使靶蛋白被泛素标记,进而被细胞内的蛋白降解系统清除。
在该研究所涉及的癌细胞实验中,PROTACs被用于靶向并降解名为BRD4的蛋白。研究人员称,一旦BRD4被破坏,癌细胞快速增殖与存活能力受到影响,从而被迫走向自毁。
递送难点:非靶向效应与分子尺寸
研究团队指出,PROTACs在应用上面临两项主要挑战:其一,BRD4对健康细胞同样重要,非靶向作用可能带来损伤;其二,PROTAC分子体积较大,难以进入细胞。
杜克大学机械工程与材料科学威廉·比文杰出教授Tony Jun Huang实验室博士生吴宇琦表示,PROTAC分子本身过大,不易穿过细胞膜;而通过SonoPIN平台,PROTACs能够进入靶向癌细胞,同时几乎不影响非靶向细胞。
SonoPIN机制:微泡坍塌引发“超声穿孔”
SonoPIN依赖预制微泡。此类微泡常用于增强超声成像对比:当微泡附着于细胞并接受较弱超声探测时,可产生回声增强图像。
研究人员进一步利用较强超声作用于微泡,使其快速坍塌,并在邻近细胞膜上诱发“超声穿孔”。团队表示,具体机制尚未完全明确,目前的假设是微泡坍塌形成高速微射流并向邻近细胞发射冲击波,从而在细胞膜上产生纳米级、短暂的孔洞,足以让PROTAC进入细胞。
Huang表示,该过程更接近“暂时且可控的机械开口”,细胞膜具有流动与动态特性,可在几分钟甚至几秒内自行修复并关闭孔洞。
参数优化与台式实验结果
在实验设计中,研究人员将合成核酸链装载到微泡上,使其能够结合癌细胞膜上存在、而健康细胞膜上不存在的特定生化受体,以实现细胞选择性。随后,团队测试多种超声频率与强度组合,以筛选出更适合打开细胞膜孔洞、促进PROTAC进入的参数。
在确定设置后,研究人员将荧光分子连接到PROTAC上进行验证。结果显示,在分别针对癌细胞与健康细胞的实验中,经过一分钟超声照射,SonoPIN处理组的细胞发光强度为传统PROTAC递送方法的七倍,表明细胞摄取了更多PROTAC。对应的生物学结果为:约半数癌细胞自毁,而约99%的健康细胞保持存活。
后续计划
研究团队表示,下一步计划在小鼠模型中测试该方法,并已就相关技术申请专利。团队设想,未来可将PROTAC与靶向癌细胞的微泡经静脉注入,并将超声聚焦于肿瘤部位,以实现更高效、且副作用较少的肿瘤杀伤。
Huang称,由于SonoPIN依赖机械方式递送而非生物吞噬过程,理论上可递送几乎任何大小的治疗药物,团队也希望进一步评估其在大型基因编辑复合物等治疗载荷中的表现。











