印度理工学院甘地讷格尔分校(IITGN)研究人员近日报告称,采用雌酮连接的BODIPY类分子作为声敏剂开展抗菌声动力疗法(SDT)具有可行性。相关初步结果已发表在《Chemistry—An Asian Journal》。
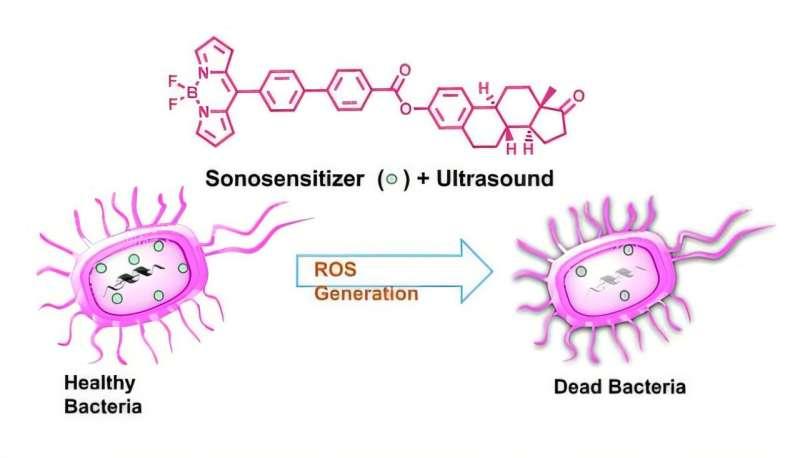
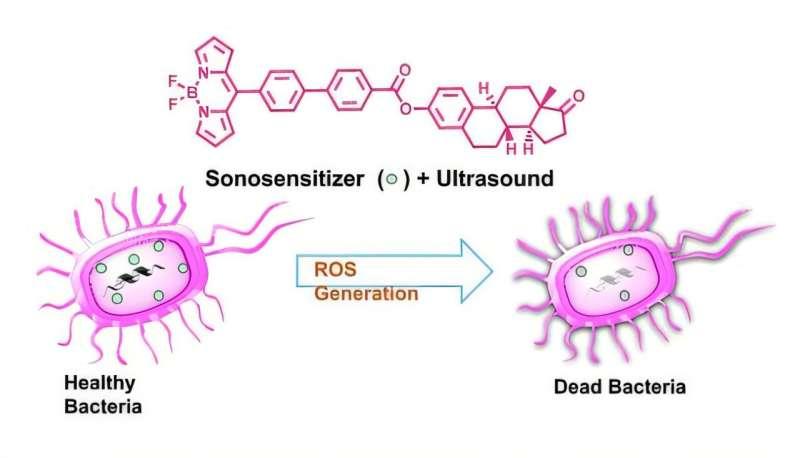
研究团队介绍,SDT并非通过抗生素抑制细菌生长,而是利用超声激活声敏剂,促使其产生具有强氧化性的活性氧(ROS),从多个层面破坏细菌结构。由于作用靶点涉及基因、蛋白质及细胞外层等多个组成部分,研究人员认为细菌较难通过单一机制形成耐受。
研究指出,超声在组织中的穿透深度可达数厘米,这一特性使SDT被视为应对局部深层感染的潜在手段。
在机理层面,团队解释称,超声在液体中传播会引发空化现象,即气泡生成并快速塌陷。气泡塌陷可释放能量并促使水分子分解,与氧气反应形成ROS;同时还可能产生微弱的声致发光。这些过程共同促进声敏剂被激活并进一步生成ROS。研究人员强调,疗效在很大程度上取决于声敏剂的选择。
IITGN化学系博士生Arjun Siwach表示,部分材料(如二氧化钛纳米颗粒)虽能高效产生活性氧,但在安全性及体内累积方面存在担忧;而一些被认为更安全的染料对超声的响应不足。
研究团队将硼-二吡咯甲烷(BODIPY)染料作为候选体系。BODIPY衍生物此前已用于光动力癌症治疗,并具备较强荧光特性,可用于生物成像;其结构也可被调控以改变能量吸收与活性氧生成能力。不过,团队指出,BODIPY在抗菌SDT方向的系统性研究仍相对有限。
在本研究中,团队设计并合成了与雌酮连接的BODIPY分子,以提升其对革兰氏阴性菌(如大肠杆菌)的作用效率。研究人员称,革兰氏阴性菌具有双层膜结构,常对疏水或体积较大的分子形成屏障;雌酮单元被用于促进分子与细菌膜结合并提高穿透能力。
团队合成了四种雌酮连接的BODIPY衍生物,并观察到这些化合物在更长波长处吸收与发射光,显示雌酮及连接体会影响BODIPY整体结构,并进而影响其在受光条件下的活性氧生成能力。
IITGN化学系教授、合成颜料实验室负责人Iti Gupta表示,实验中EBD-1表现最为突出,在超声照射后可产生大量ROS并实现杀菌效果。她称,在针对大肠杆菌的体外实验中,超声、EBD-1与临床批准的微泡联合使用可清除99.9%的细菌。
研究同时说明,微泡为带有蛋白质或脂质壳的微小气泡,可作为空化核增强气泡生成与塌陷效应。团队报告称,所有实验条件下温度均控制在42°C以下,提示观察到的抗菌作用主要来自化学与机械效应,而非热效应。
IITGN电气工程系副教授、医学超声工程实验室负责人之一Himanshu Shekhar表示,该研究展示了可穿透细胞的BODIPY分子与超声驱动空化结合用于抗菌SDT的可行性,并指出后续仍需通过动物实验与临床试验验证。
研究人员称,该方向与印度《抗微生物耐药国家行动计划(2025–2029)》所强调的需求相契合。该计划由印度政府推动,采取多部门“一体健康”框架,旨在通过监测、信息传播与创新研究应对耐药细菌威胁。
团队表示,下一步研究可围绕声敏剂结构优化及联合治疗策略展开,包括微泡类型与声学条件等参数的进一步调整,并推进向动物与临床研究的转化验证。











