大量在研药物面临一个基础但关键的障碍:水中溶解度不足。由于口服给药仍是多数治疗中最常用的方式,药物活性成分需要先在胃肠道液体中溶解,才能进一步被吸收入血。若溶解速度过慢或溶解不完全,药效可能受到影响。相关研究将这一问题称为“溶解度危机”,并指出其已成为现代药物开发的重要瓶颈之一,影响范围可达90%的活性化合物。
通过无定形化提升溶解度的既有路径与限制
为改善溶解度,药物科学领域常通过改变药物的物理形态入手。多数药物天然以晶体状态存在,分子排列规则且结构稳定,不利于快速溶解。将晶体转变为无定形状态(分子无序排列)被认为是提升水溶性的一种有效方式。
在实践中,蒸发/冷凝(EV)法是一种常见手段,即先将药物溶解于有机溶剂,再通过蒸发等过程使药物分子吸附到介孔硅(MPS)等多孔材料上,以抑制重新结晶并维持无定形状态。不过,EV法对强效有机溶剂的依赖带来健康与环境方面的顾虑。

研究提出密封加热法:以气相实现无溶剂负载
为寻找更可持续的替代方案,日本东京理科大学(TUS)药学部羽川岳久教授团队探索了无需有机溶剂的介孔硅药物负载方法。团队在《药学杂志》(Journal of Pharmaceutical Sciences)发表论文,介绍“密封加热”(SH)法:该方法绕开液态化学品,通过气相过程实现药物负载。
论文作者包括:前东京理科大学兼职讲师、现名古屋市立大学教授河野弥生;前东京理科大学兼职助理教授广濑香织和小泽智裕;2021年东京理科大学硕士毕业生野村一也;以及Kaken Pharmaceutical株式会社CMC中心制剂部的名取信行先生和大场拓真博士。
在SH法中,研究人员将介孔硅与药物粉末进行固体混合,并置于轻微加热的真空容器内。该方法的前提是药物在相应条件下能够发生升华,即由固态直接转为气态。药物进入气相后,可吸附到硅孔内表面,并在孔结构限制下保持无定形状态,从而提升溶解度。
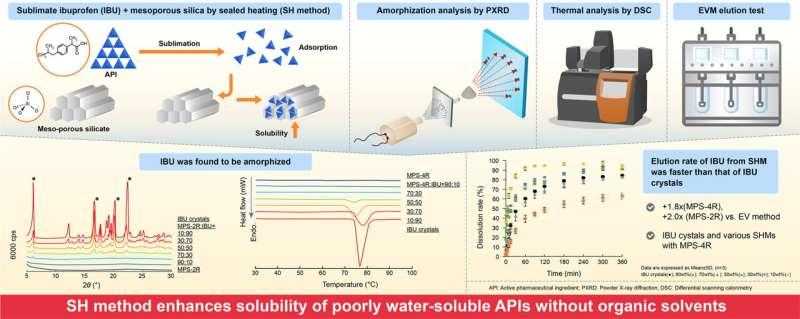
布洛芬对比测试:最佳条件下溶出速度提升2.7倍
研究团队选取具有升华特性的布洛芬作为代表药物,对比了SH法、简单物理混合以及传统EV法的效果,并使用分析技术跟踪药物结晶度、孔结构变化以及药物与介孔硅之间的分子相互作用。
结果显示,在最佳条件下,SH法制备样品的表现可与EV法样品相当。布洛芬吸附至介孔硅后,在低至中等药物负载量时可完全呈无定形状态,且在孔容较大的硅材料上表现更为突出。
溶出测试进一步显示,最佳介孔硅配方在前10分钟内释放布洛芬的速度为原始晶体药物的2.7倍。化学分析同时确认,布洛芬分子保持完整,且未与介孔硅载体发生不良化学反应。
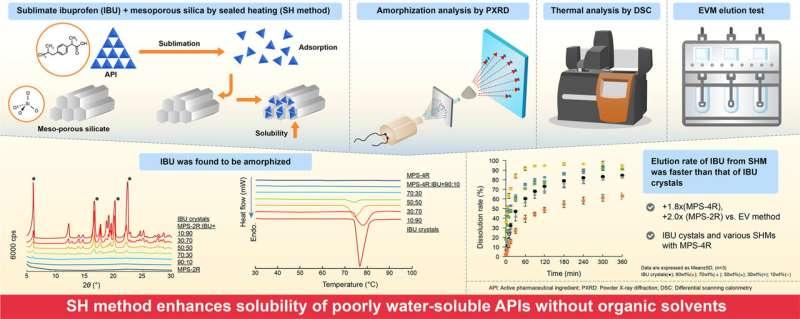
环境与工艺层面的意义及适用边界
研究团队认为,上述结果使SH法成为应对“溶解度危机”的一种潜在方案。羽川岳久表示,药物能够通过气相直接负载到介孔硅上,使SH法成为一种无需有机溶剂、相对环保且安全的药物负载技术。
研究还指出,无溶剂特性可能有助于简化制药工艺,并在成本与监管负担方面带来潜在影响。由于该过程依赖物理吸附而非化学键合,团队提出同一载体上进一步吸附其他药物、用于制造复方药物的可能性。
在适用范围方面,研究团队提到,该方法还可用于负载对羟基苯甲酸类、甲芬那酸、乙苯酰胺、氟芬那酸和阿司匹林等抗炎药物,并可被多孔材料处理企业及介孔硅制造单位采用。不过,SH法的适用对象仍受限于可升华药物。研究认为,即便存在这一边界,该工作仍展示了药物制剂技术的一种新方向,为将有潜力的药物分子转化为可用药物提供了更清洁、简化的路径。











