将人工智能与先进机器人技术结合、构建自驱动实验室(SDL),正被用于应对分子发现中的效率与规模难题。多伦多大学莱斯利·丹药学院研究人员牵头的一项研究近日发表于《Cell》,介绍了一套名为LUMI-lab的SDL系统,并报告其在mRNA递送材料筛选中发现:此前未被认为与mRNA递送相关的溴化脂质尾部,可作为提升转染效率的关键设计特征。
研究团队表示,LUMI-lab(大规模无监督建模后迭代实验)由多伦多大学加速联盟的AC翻译研究资助支持,核心做法是将分子基础模型与自动化机器人实验系统整合,在闭环流程中进行“设计—合成—测试—学习”的迭代优化。团队在实验中意外识别出一类新的mRNA增强脂质,即带有溴化尾部的可电离脂质。
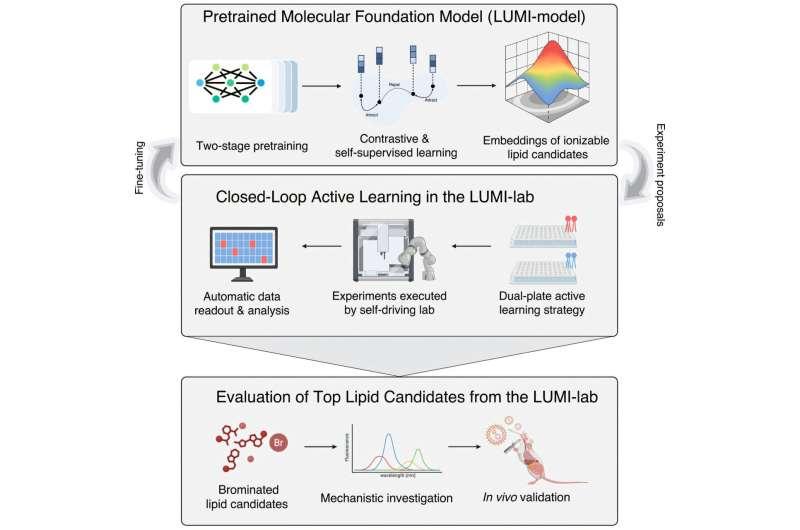
据多伦多大学莱斯利·丹药学院药剂学与药物递送GSK主席、同时为多伦多大学健康网络公主玛格丽特癌症中心附属科学家的李博文介绍,在10个主动学习周期内,LUMI-lab合成并测试了超过1700种新的脂质纳米颗粒(LNP)。结果显示,溴化尾部的可电离脂质在将mRNA递送至人体肺细胞方面的效率高于已批准的基准材料。李博文称,该系统的关键进展在于其在没有先验假设或研究人员指示的情况下,独立识别出“溴化”这一重要且具有意义的分子设计特征。
研究指出,尽管mRNA治疗是增长最快的药物形式之一,但目前仍主要依赖LNP将mRNA安全递送至人体目标区域;截至目前,仅有三种LNP获得美国食品药品监督管理局(FDA)批准。研究团队认为,类似LUMI-lab的平台可通过加速下一代LNP的发现、拓展材料设计空间,为更多治疗应用提供支持。
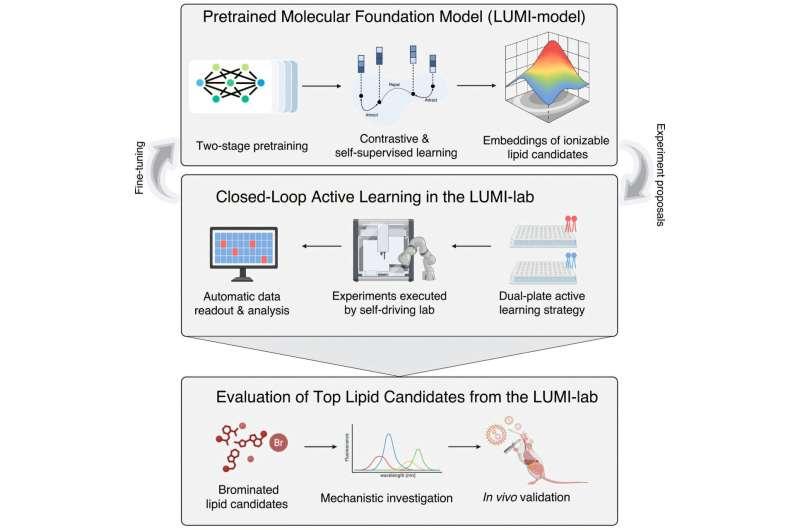
研究同时提到,SDL模式对高质量数据依赖较强,而在mRNA治疗开发与递送等新兴领域,历史数据稀缺仍是主要障碍。为应对数据不足,团队采用基础模型路径,并对LUMI进行了超过2800万分子结构的预训练,使其在进入具体任务前先学习通用化学模式与结构。李博文表示,当该模型被纳入主动学习框架后,可在闭环工作流程中持续优化,从而进一步提升预测准确性。
在临床前模型测试中,部分新发现脂质的表现优于Moderna新冠mRNA疫苗所用脂质。研究显示,溴化脂质在LUMI-lab使用的化合物库中占比约8%,但在表现最佳的候选者中占据一半以上。研究还称,溴化脂质呈现出与临床基准脂质相似的安全性,支持其后续治疗开发潜力。
李博文表示,下一步团队将扩展LUMI-lab,用于优化多项临床相关特性,除递送效力外,还包括安全性、耐受性和组织选择性;并希望通过进一步闭合人工智能预测与自动化实验之间的循环,缩短新型脂质材料的设计周期,拓展mRNA治疗的化学空间。












