密歇根大学研究人员报告称,细胞在执行程序性细胞死亡过程中,可能通过一种此前未被描述的分子组织方式来帮助保护宿主生物。研究团队表示,这一机制所需的“构建模块”在生命树中广泛存在,相关发现有望为理解植物韧性以及人类免疫反应提供新的研究线索。
该项目高级负责人、密歇根大学分子、细胞与发育生物学系(MCDB)教授单立波表示,这项发现可能对多个生物学研究方向产生影响。研究由MCDB教授何平共同领导,成果已发表在《自然》杂志上。
程序性细胞死亡的“尺度”问题
研究人员指出,个体细胞保护宿主免受疾病侵害的一种方式,是在感染或受损时通过自我牺牲阻断病原体扩散。何平表示,程序性细胞死亡是一种有效但需要精细控制的防御策略:清除足够多的受损细胞有助于遏制疾病发展,但若反应过度,也可能波及健康细胞并损害宿主。
何平称,在植物和哺乳动物中,细胞死亡与抵抗力相关,但关键在于将防御反应限制在有限区域。过去几十年,研究人员已在植物中鉴定出启动细胞自毁序列的基因和蛋白质,并发现其中部分要素与哺乳动物细胞的相关机制存在共通之处。不过,科学界仍在尝试完善这一过程的分子层面“协同图谱”,以解释细胞如何在触发死亡反应的同时避免失控。
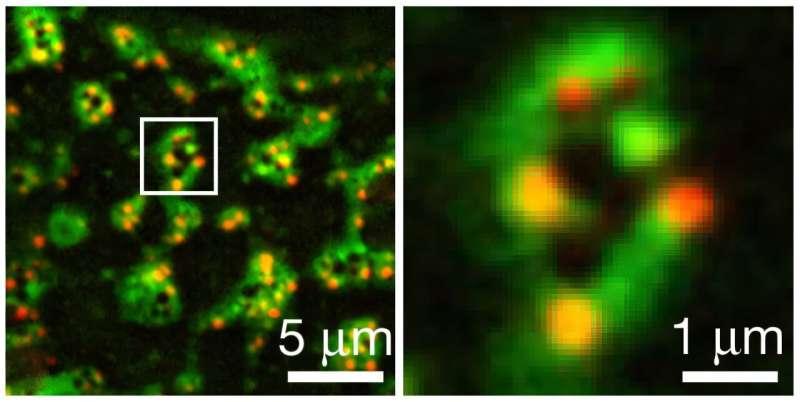
在细胞膜上观察到环状组装
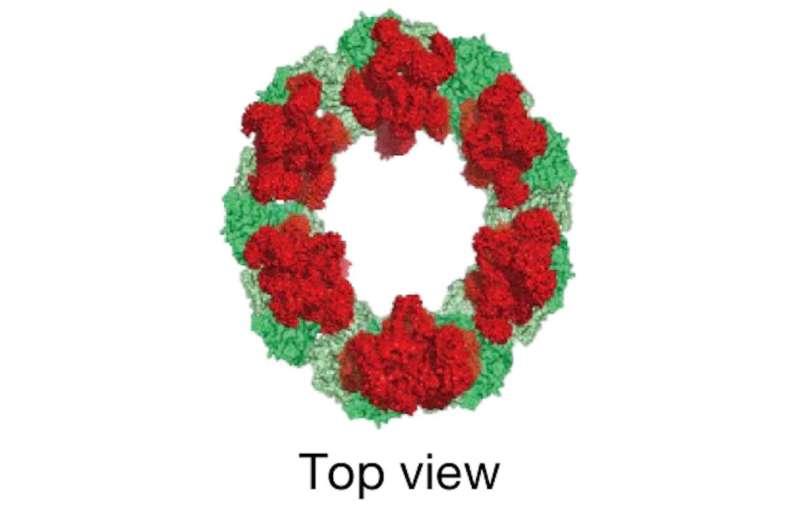
研究团队介绍,免疫学领域近期研究显示,参与该过程的蛋白质可聚集形成能够运输钙离子的通道,但仅有这些通道并不足以启动细胞死亡。在此基础上,何平、单立波及其团队进一步报告称,这些通道会在细胞膜上被组织成环状结构。
单立波表示,团队首次展示了这些通道如何在细胞膜上形成类似“花环”或“项链”的结构:该结构由结合于细胞膜的蛋白质以及6个跨膜定位的通道组成。相关观察基于拟南芥和烟草两种常用植物模型系统,并借助高分辨率全内反射荧光显微镜完成。
后续研究聚焦结构功能与信号传递
研究人员称,这一发现也带来新的问题,包括该环状结构的具体功能及其作用机制。团队目前提出的假设是,环状结构可能促进与邻近细胞的通讯并发送炎症信号,从而以更具针对性的方式启动细胞死亡。
单立波表示,团队正与密歇根大学生命科学研究所以及其冷冻电子显微镜实验室合作,进一步解析这些环状结构的细节,并研究可能通过该结构“泄漏”的物质以及支持其形成的因素。研究人员同时指出,相关发现可能为增强植物韧性以及研究人类细胞死亡失控相关疾病提供新的研究路径,但仍有多项关键问题有待回答。











