碱基编辑技术在不到十年间从实验室研究推进至临床应用,已被用于探索治疗严重或致命疾病的路径。该技术通过对DNA进行化学修饰实现定点改变,由加州大学圣地亚哥分校(UC San Diego)生物化学与分子生物物理系副教授Alexis Komor开发。
尽管碱基编辑已取得多项进展,但作为相对较新的基因编辑手段,研究人员仍在持续优化其性能,重点包括在提升目标编辑效率的同时降低不良编辑发生率。Komor团队在《自然生物技术》发表的最新研究,提出一种可最大限度减少“旁观者编辑”的方法。
旁观者编辑与“编辑窗口”难题
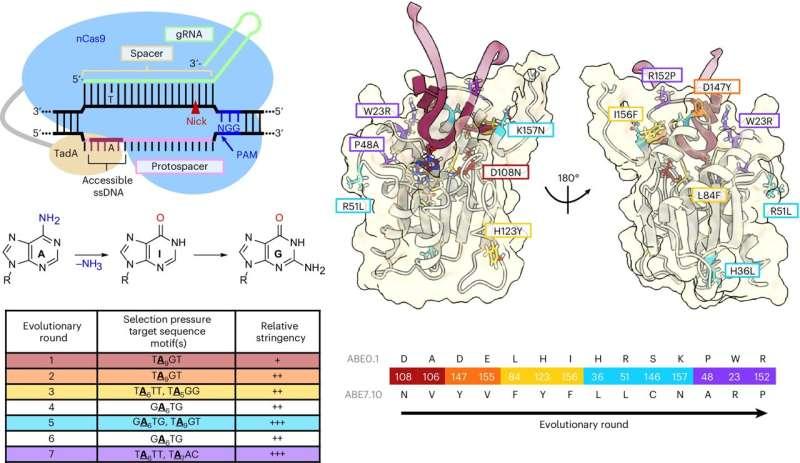
碱基编辑通常在DNA单链上完成。以腺嘌呤碱基编辑器(ABE)为例,其可将目标腺嘌呤(A)核苷酸编辑为鸟嘌呤(G)。但当目标位点附近存在多个A碱基时,编辑器可能在完成目标编辑的同时改写周围碱基,形成“旁观者编辑”。相关改变可能是无害或“沉默”的,也可能带来不良后果,甚至导致细胞死亡。
降低旁观者编辑的一种常见思路是缩小“编辑窗口”,即编辑器能够有效作用的碱基范围。不过,既有研究显示,编辑窗口变窄往往会伴随目标编辑效率下降。Komor表示,在治疗应用场景中,同时优化效率与安全性至关重要;如果高效目标编辑伴随其他不良编辑,相关工具将难以安全用于治疗。
从ABE7.10出发构建“最小进化”编辑器
在该研究中,Komor实验室前博士后、化学专业校友Mallory Evanoff将工作重点放在ABE的早期版本ABE7.10上。与近期开发的ABE8.20和ABE8e相比,ABE7.10的编辑窗口更窄,但编辑效率较低;而ABE8系列变体因目标编辑效率更高而被更广泛使用(包括临床试验中),但其旁观者编辑水平也更高。Evanoff的目标是兼顾两者优势。
研究介绍,为实现A到G的转换,ABE7.10依赖一种经过14处点突变工程改造的酶,这些突变此前被认为对有效碱基编辑至关重要。相关突变的引入与筛选通过在大肠杆菌细胞中进行的定向进化完成,但各突变对编辑活性的具体贡献并不清晰。
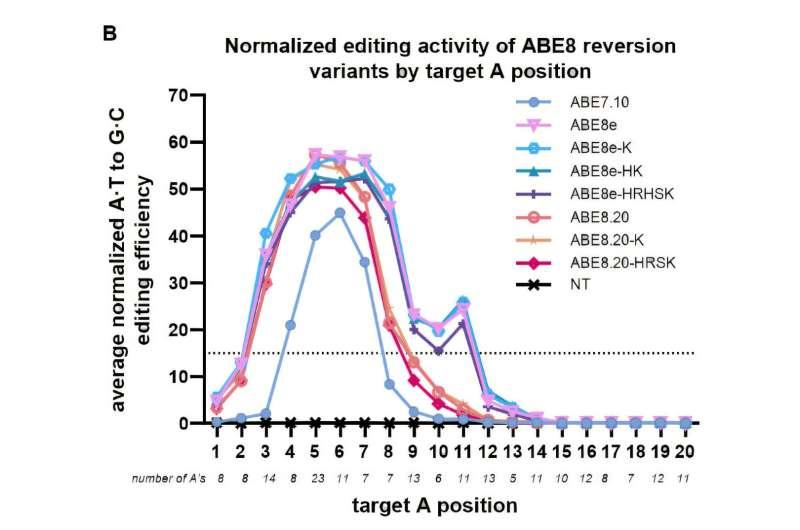
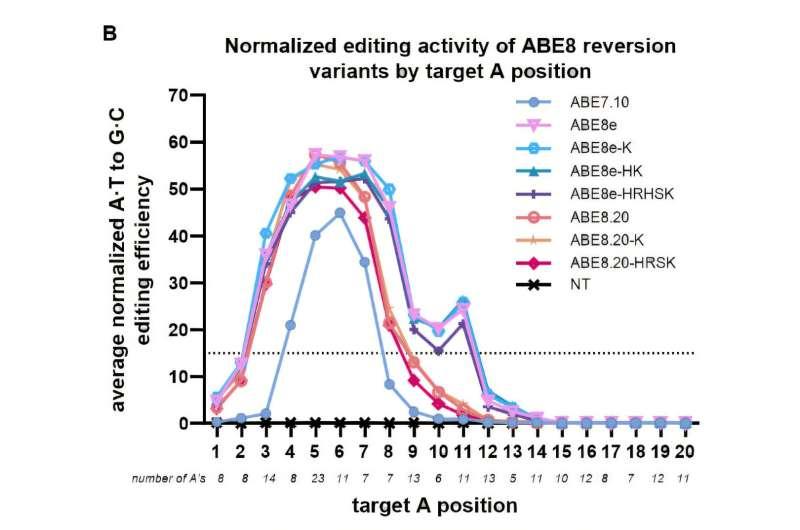
为解析这些影响,Evanoff采用逆转分析方法,将14个突变分别单独恢复为原始“野生型”序列,并在人体细胞与大肠杆菌细胞中分别表征这些单独逆转突变的活性。她观察到,部分突变在细菌中表现相似,但在两种宿主系统中的效果并不一致。考虑到多数研究者在人体细胞中使用ABE,Evanoff最终筛选出五个在人体细胞中单独逆转后对编辑活性无影响或可提升活性的突变,并将其组合,构建出“最小进化ABE”(ME-ABE)。
研究结果显示,ME-ABE在保持较窄编辑窗口的同时,获得了与更常用的两种ABE8变体相近的编辑活性。Komor表示,这项工作首次实现了对“效率”和“编辑窗口”两项特性的解耦;在其他研究中,提高编辑活性往往伴随编辑窗口变宽,从而增加旁观者编辑。
用于模拟与纠正遗传突变的研究工具
研究人员指出,个体之间可能存在数百万种遗传变异,其中部分会导致严重或致命的遗传疾病。识别哪些突变或突变组合与疾病相关,是一项需要逐步验证的工作。Evanoff表示,构建更精准的工具有助于在模型生物中安装特定突变以开展验证,也有助于更具体地解析多突变背景下哪些变化与症状或疾病相关。
Evanoff将ME-ABE形容为“双刃剑”工具:一方面可帮助研究者更好地模拟并理解潜在致病突变,另一方面也可用于实施更具针对性的纠正,为开发面向特定疾病的个性化治疗方案提供工具基础。
根据研究描述,Komor与Evanoff仍在继续开发新的碱基编辑器,重点包括在哺乳动物细胞而非细菌中进行进化,并希望ME-ABE能成为其他研究者进一步开发高效基因编辑工具的起点。











