许多生物功能依赖蛋白质三维结构形成的受体位点与配体分子之间的特异性结合。当受体结构因突变等原因发生改变,或配体出现偏差时,相关生物过程可能受损并引发疾病。在药物发现中,研究人员通常通过筛选流程寻找能够与这些靶点位点匹配的候选分子。
《PNAS Nexus》近日发表的一项研究提出一种无细胞筛选平台,旨在提升肽段筛选效率,并扩展到以往在细胞体系中难以处理的高毒性蛋白或非生理条件下的筛选场景。研究的核心做法是制备携带单一肽段的磁珠,在不依赖活细胞的情况下完成展示与筛选。
研究团队指出,传统依赖活细胞表达肽段的方式可能出现产量波动,从而影响数据一致性。与传统方法相比,该无细胞方案在筛选效率上实现超过十倍的提升;同时,平台可在高温、高盐等条件下开展筛选,研究人员认为这有助于缩短药物开发中先导化合物发现所需时间。
以无细胞展示为基础的筛选平台
寻找能够与特定靶标精确结合的蛋白质或肽段,是新药开发与疾病诊断的重要技术基础。围绕这一目标,业界已发展出多类“展示技术”用于从大量候选序列中筛选结合分子。近年来,无需使用大肠杆菌或酵母等活细胞、在试管中直接合成蛋白质的“无细胞蛋白质合成”技术应用增多,其特点是免去细胞培养环节,实验条件更灵活。
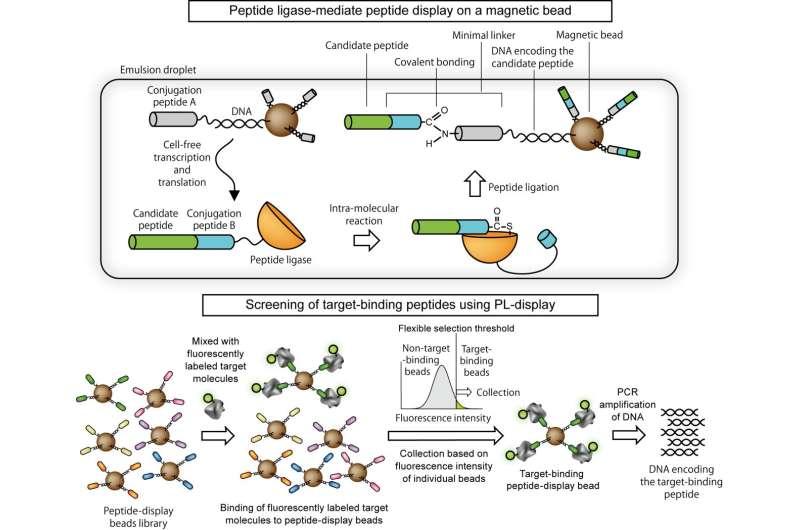
本研究中,iCONM研究团队将无细胞合成得到的蛋白质固定到可被磁铁吸附的小颗粒表面,并通过逐颗粒测量的方式评估磁珠与靶标的结合强度,以筛选出表现更优的候选分子。
“PL-display”方法与固定机制
研究利用“肽连接酶”可将肽段连接的特性,开发出一种将肽段及其模板DNA共同固定在磁珠表面的技术。具体而言,研究通过仅含九个氨基酸的短连接段,将肽段(短蛋白片段)与对应DNA牢固连接到磁珠上,并将该方法命名为“PL-display”。研究强调,该方法的关键特征是:单个磁珠仅展示一种肽段及其对应DNA,且整个流程不需要活细胞参与。
在筛选环节,研究使用FACS(荧光激活细胞分选)设备对磁珠逐个检测,并依据荧光强度等数值指标进行分选,从而实现对候选磁珠的精确筛选。
概念验证:低丰度目标的分离与富集
为验证方法有效性,研究首先将两种标记肽HA-tag与His-tag的DNA等量混合,并分别展示到磁珠上;随后加入仅与各自肽段结合的荧光标记抗体。与靶标结合的磁珠呈现更强荧光信号,研究人员据此分选出荧光最强的磁珠,并对其携带的DNA进行PCR扩增以确认序列来源。
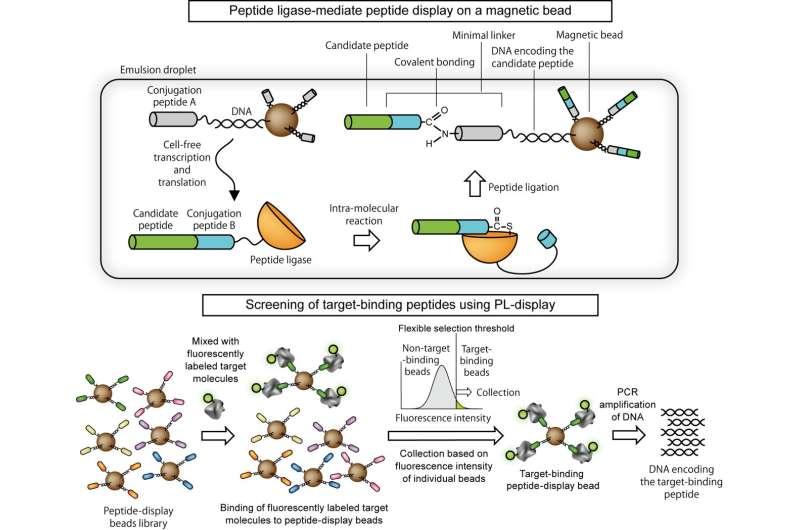
研究结果显示,分选能够准确提取目标肽段对应基因。进一步实验中,即使HA-tag基因在混合物中的比例仅为0.01%(万分之一),研究人员也表示仅通过一次筛选即可将HA-tag基因完全分离出来。此外,在约170万个随机序列肽段的库中,研究称仅用两轮筛选便收集到能够与抗HA-tag抗体结合的肽段。
研究还指出,通过基于单颗磁珠荧光强度设定更严格的回收阈值,可在单次分选步骤中实现约1万倍的浓缩效率,并认为这有助于在更复杂、多样的肽段群体中快速识别目标序列。
无细胞磁珠筛选在条件适配性上的特点
研究团队表示,由于采用无细胞蛋白质合成,平台不受细胞生长条件限制,也可减少因单个细胞蛋白产量差异带来的影响;同时,该体系可用于研究对细胞有害的蛋白,或在非正常生理环境下开展实验。
在结构稳定性方面,研究称肽段与模板DNA通过不易断裂的强键连接,且每个磁珠仅展示一种蛋白质,使其在剧烈洗涤或高盐浓度等条件下仍能保持稳定,从而更精确地评估“单颗磁珠与靶标的结合强度”。借助FACS按荧光强度分选,研究人员可设置如“仅回收超过某一亮度阈值的磁珠”等标准。研究认为,该机制不仅可用于筛选结合力更强的分子,也可用于筛选结合强度处于特定区间、符合需求的候选分子。
潜在应用方向
研究团队预计,基于PL-display的超高通量靶标结合筛选可用于药物发现、诊断与生物材料开发等场景,包括治疗性与诊断性肽段、低分子抗体的筛选;也可用于面向非生理环境的工业蛋白开发,并与基于磁珠平台的自动化与机器人技术结合,实现更高速的筛选流程。











