海德堡大学药学与分子生物技术研究所研究人员提出一种模块化设计策略,使蛋白质活性能够借助热敏开关在细微温度变化下实现精确调控。研究团队表示,该策略可将温度感受域整合进多类蛋白质之中,不受蛋白质功能或空间结构差异的限制。
为热遗传学提供通用化路径
研究团队由多米尼克·尼奥佩克(Dominik Niopek)教授和扬·马索尼(Jan Matschon)博士牵头,相关成果已发表在《自然化学生物学》(Nature Chemical Biology)。研究人员指出,蛋白质作为细胞内的“分子机器”,参与并调控几乎所有生命过程,且反应具有高度动态性。为了更清晰地理解这些过程及其时间顺序,实验工具需要能够在可控条件下精确改变单一参数。

在此背景下,研究人员将可“开关式”调节的蛋白质视为理想对象,并强调热敏蛋白开关的优势在于:温度可实现时空上的紧密控制,同时作为信号可穿透组织或复杂生物样本,从而为非侵入式调控细胞过程提供可能。
构建对生理温度窗口敏感的变构热开关
研究人员表示,以往对蛋白质进行温度依赖性控制被认为技术门槛较高、适用范围受限,许多方法主要依赖基因表达层面的间接调控。此次工作中,团队将植物感受域的优化变体整合到天然蛋白质中,开发出“变构热开关”。
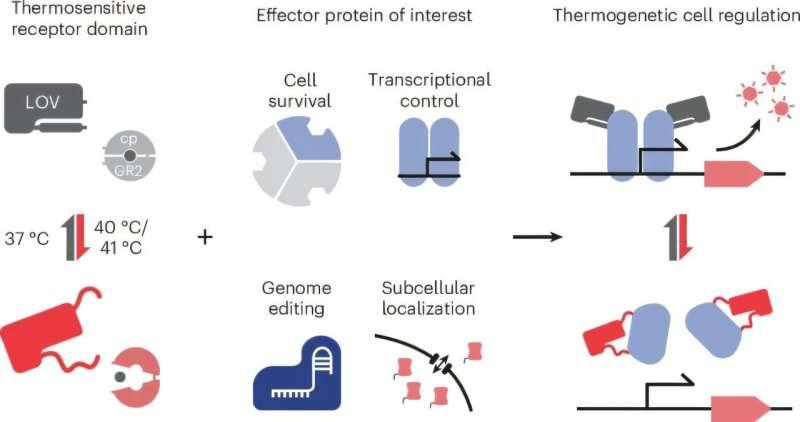
据介绍,这类开关可在人体细胞生理温度窗口(37°C至40°C)内对极小温度变化产生响应,从而改变蛋白质活性,并实现对细胞功能的紧密控制。博士生安-索菲·克罗尔(Ann-Sophie Kroll)表示,团队的目标是让温度成为一种更通用的蛋白质控制刺激源。
为验证策略可行性,研究人员先在大肠杆菌中进行测试与优化,随后将该方法转移至哺乳动物细胞,并据此设计出温度可控的CRISPR-Cas基因编辑器,使其活性能够被精细调节。尼奥佩克表示,借助这些变构热开关,研究人员可以在不主动干预细胞其他过程的情况下,对细胞功能进行直接且可逆的控制。
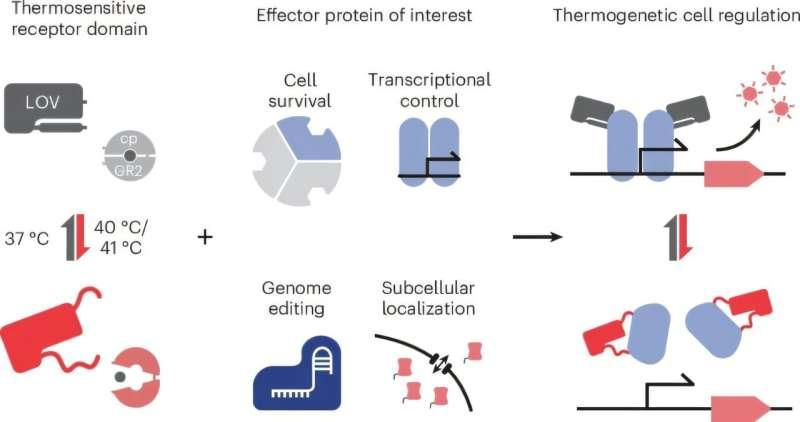
模块化设计支持多类温控蛋白开关开发
研究人员称,该方法的关键特征之一是模块化程度高。除最初采用的感受域外,团队还将另一种同样对温度变化作出响应的受体模块成功整合进蛋白质中。研究人员认为,这一模块化设计策略可作为通用蓝图,用于构建温度控制的蛋白质开关,并可在不依赖蛋白质功能或空间结构的前提下实现整合。
马索尼表示,团队希望推动热遗传学发展为更全面且适用范围更广的技术,未来能够仅通过热量对几乎所有蛋白质进行精确调控。尼奥佩克补充称,这一策略也显示出面向未来生物医学应用的潜力。











