一项最新研究指出,L1td1这一在进化过程中由长散在核元件1(LINE-1)逆转录转座子“驯化”而来的蛋白,可能在维持多能干细胞(PSCs)状态中发挥关键作用。研究显示,当L1td1缺失时,细胞内全能性相关基因及内源性逆转录病毒(ERVs)表达被激活,多能干细胞可自发回退至类似全能的2细胞样(2C样)状态,呈现胚胎发育最早阶段的特征。
该研究由中国科学院广州生物医药与健康研究院(GIBH)刘新国教授团队完成,成果近期发表于《Cell Discovery》。
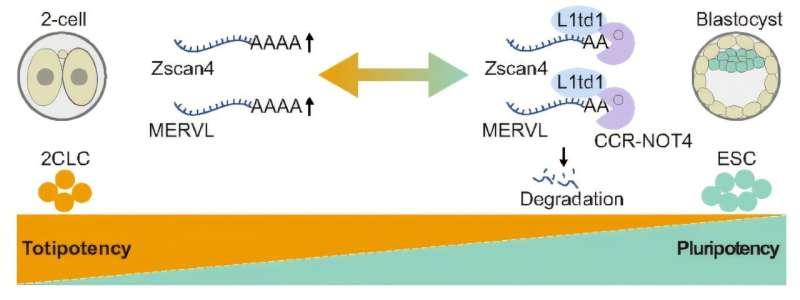
研究团队指出,从全能性向多能性的转变是早期胚胎发育中的基础事件之一,其典型特征包括:全能性基因以及在合子基因组激活(ZGA)期间被激活的特定逆转录转座子逐步被沉默。尽管相关转录与表观遗传层面的调控机制已有较多研究,但转录后调控,尤其是RNA降解在这一过程中的作用仍缺乏充分认识。
L1td1被描述为哺乳动物中唯一一个由“跳跃”型LINE-1逆转录转座子驯化而来的蛋白编码基因,并在多能干细胞中呈高表达。为明确其在细胞命运转变中的功能,研究团队使用小鼠与人类多能干细胞模型开展实验,结果显示L1td1在阻止细胞获得全能性方面具有决定性作用。
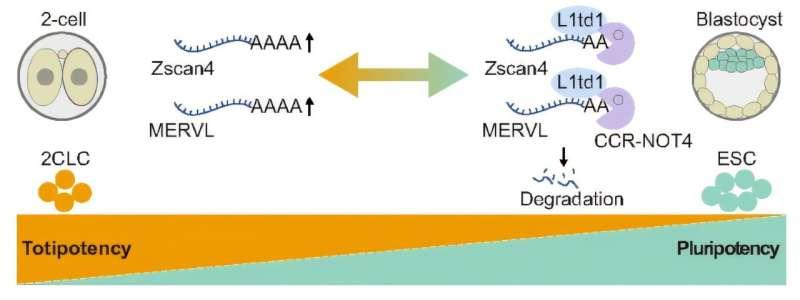
在机制层面,研究发现L1td1可招募CCR4-NOT脱腺苷酸酶复合物,选择性靶向并降解与全能性维持密切相关的RNA转录本,其中包括Zscan4基因家族,以及MERVL-int、MT2_Mm等ERVs相关转录本。研究还报告,L1td1同样会靶向其进化祖先LINE-1的RNA并促进其降解。研究团队认为,通过清除上述转录本,L1td1可抑制细胞回退至2C样状态,从而维持多能性身份。
研究作者表示,这些结果揭示了一种新的调控路径:被驯化的转座子蛋白通过CCR4-NOT介导的RNA降解,将转座子沉默与细胞命运决定联系起来,并凸显RNA稳定性控制在早期胚胎发育及基因组防御中的作用。
论文同时指出,该发现为理解病毒元件与宿主发育调控之间的进化相互作用提供了新的线索,并为再生医学及异种器官再生等领域中诱导全能性研究提供潜在思路。











