约翰霍普金斯基梅尔癌症中心、布隆伯格~基梅尔癌症免疫治疗研究所及约翰霍普金斯布隆伯格公共卫生学院的研究人员报告称,一种参与蛋白质翻译过程的酶对循环免疫细胞单核细胞成熟为组织驻留巨噬细胞具有关键作用。组织驻留巨噬细胞通过清除死亡细胞和组织碎片等方式维持器官稳态。
研究显示,在缺乏该酶的情况下,单核细胞仍可进入组织并启动分化,但无法完成成熟过程,导致组织维护能力受损。研究人员观察到,相关组织出现免疫细胞持续浸润,炎症反应增强,而非形成有效的修复。
该研究发表于《自然》。论文指出,脱氧羟脯氨酸合酶(DHPS)对多个器官中的巨噬细胞分化与长期存活均不可或缺,涉及肺、肝、脑、肾、心脏以及腹膜腔等。研究团队通过一系列小鼠模型发现,DHPS调控一套与组织类型无关的核心程序,使巨噬细胞能够与局部环境建立黏附与互动,并执行维持组织平衡的功能。
研究负责人、约翰霍普金斯大学肿瘤学系及生物化学与分子生物学系布隆伯格杰出教授Erika Pearce表示,组织驻留巨噬细胞在清除死亡细胞、修复损伤和维持器官平衡方面具有重要作用;当这些细胞无法正常成熟时,相关保护功能会丧失,并与炎症和疾病表现相伴。
研究进一步解释了DHPS影响免疫细胞成熟的机制。组织驻留巨噬细胞在胚胎发育期间形成,通常可在局部自我更新;但在受伤或细胞丢失时,骨髓来源的单核细胞会被招募进入组织,并需要分化为成熟巨噬细胞以恢复正常细胞群体。研究发现,当在髓系细胞中删除DHPS后,组织内虽仍可检测到巨噬细胞,但其缺乏成熟组织驻留巨噬细胞的典型特征与功能。
论文第一作者、Pearce实验室前研究生Gustavo Carrizo称,单核细胞的迁移与浸润仍会持续发生,但在缺乏DHPS时无法转变为承担组织维护与修复所需的成熟巨噬细胞。
研究人员将上述缺陷追溯至多胺-羟脯氨酸通路。对基因活性、蛋白质产量及蛋白质合成机制的分析显示,DHPS对一部分与细胞黏附、信号传导及组织互动相关基因的高效翻译至关重要。研究称,缺乏DHPS会使巨噬细胞难以表达用于在组织中“锚定”自身并响应局部信号的关键蛋白。
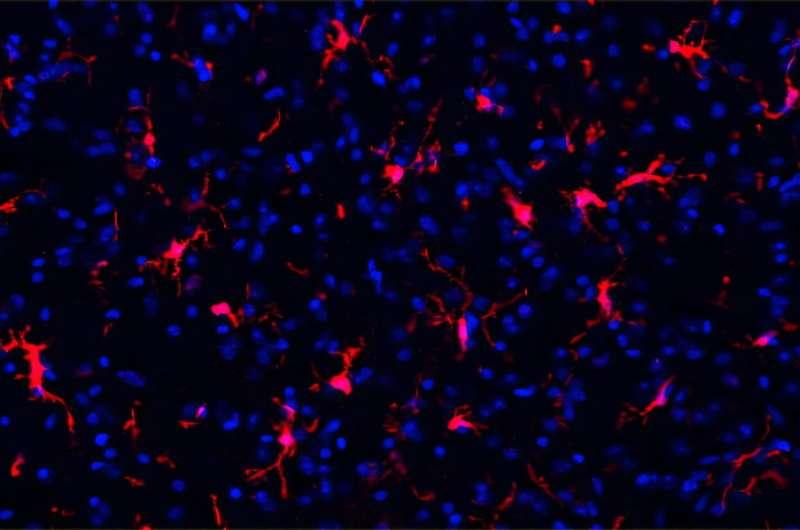
成像结果显示,缺乏DHPS的巨噬细胞在组织中的形态与定位异常;功能检测则提示其在清除死亡细胞与组织维护方面存在缺陷。研究举例称,在肺部,这种功能障碍与肺泡表面活性物质积聚以及免疫细胞浸润相关;在肝脏,急性巨噬细胞耗竭后未能恢复,伴随血管破坏与组织损伤。
伊坎医学院免疫学与免疫治疗助理教授、共同通讯作者Daniel Puleston表示,鉴于组织驻留巨噬细胞在癌症、伤口愈合、纤维化及炎症性疾病中发挥作用,该通路可能与多种疾病相关,也可能与衰老过程中常见的炎症与组织修复受损有关。
研究作者认为,这些结果将蛋白质翻译的代谢调控与免疫细胞分化及组织稳定性联系起来,提示DHPS是单核细胞向长寿且功能完善的组织驻留巨噬细胞转变所需的核心细胞内调控因子,且其作用不依赖具体组织类型。研究团队表示,下一步将识别全部依赖DHPS的蛋白质,并进一步明确该通路在特定疾病中如何影响巨噬细胞行为。











