许多疾病被认为起源于细胞层面的异常,并牵涉多种分子过程的相互作用。研究人员指出,传统研究往往依赖对大量细胞信号的平均化分析,难以精确捕捉单个细胞的细微变化,从而可能错过疾病早期信号。
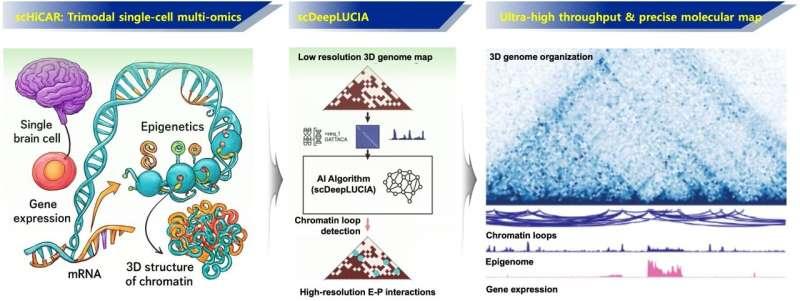
生物科学系郑仁京教授研究团队与杜克大学刁亚锐教授团队合作,开发了名为scHiCAR的技术(单细胞Hi-C结合转座酶可及染色质测定和RNA测序)。研究团队称,该方法可在同一单个细胞内同时测量基因表达信息(转录组)、表观基因组特征以及三维基因组结构,并具备超高通量与高精度的特点。
相关成果已发表在《自然生物技术》杂志。
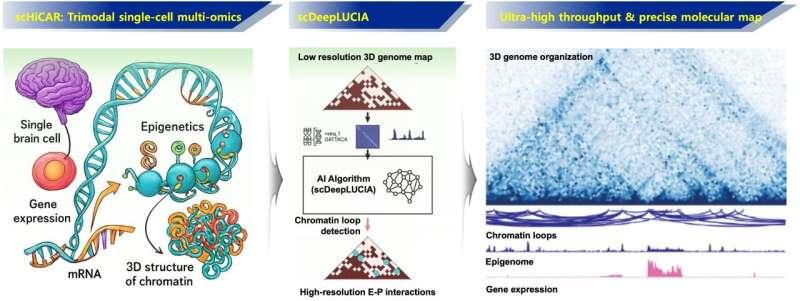
研究团队表示,细胞状态的判定不仅取决于哪些基因处于活跃状态,还与基因为何被激活的调控环境以及其在细胞核内的空间组织方式有关。此前的技术路径通常需要从不同细胞分别获取转录组、表观基因组和三维基因组信息,再进行事后匹配,这一过程可能造成细微差异被扭曲或遗漏。
为解决上述问题,研究团队引入三模态多组学的一体化测量方案,使三类遗传信息能够在单细胞内同步检测。团队同时结合人工智能方法进行数据分析,以提升测量结果的准确性与重复性,并将其整合为统一的平台化流程。
在成本方面,研究团队称已将单细胞分析成本降至每个细胞约0.04美元(约合50韩元)。基于该技术,团队构建了160万个小鼠脑组织细胞的高分辨率分子图谱,并表示这将有助于在细胞层面更精确地定位疾病相关基因在何时、何地以及在何种空间结构背景下被激活或关闭。
研究团队还将scHiCAR应用于脑组织与肌肉再生过程,报告称在22种主要细胞类型中观察到不同的基因运作规律。其中特别提到,团队实现了对肌肉干细胞再生过程中基因三维结构动态变化的实时追踪,并进一步观察这些变化与细胞命运之间的关联。
郑仁京教授表示,这项研究使研究从“观察细胞”推进到更精细地读取细胞内基因组信息,并称其有望推动对帕金森病、癌症等复杂疾病发育机制的阐明以及患者特异性新药靶点的识别。











