无义介导的mRNA降解(NMD)被认为是细胞内重要的分子质量控制过程之一,可避免产生有缺陷或不完整的蛋白质。近日,研究人员进一步厘清了该系统中触发缺陷mRNA切割的关键机制。
蛋白质合成通常以DNA信息转录生成mRNA为起点。NMD机制会对mRNA进行检查,并选择性清除存在错误的转录本。此前,SMG5与SMG6等关键因子已被确认参与NMD过程,但缺陷mRNA的关键切割步骤如何被激活,长期缺乏明确解释。
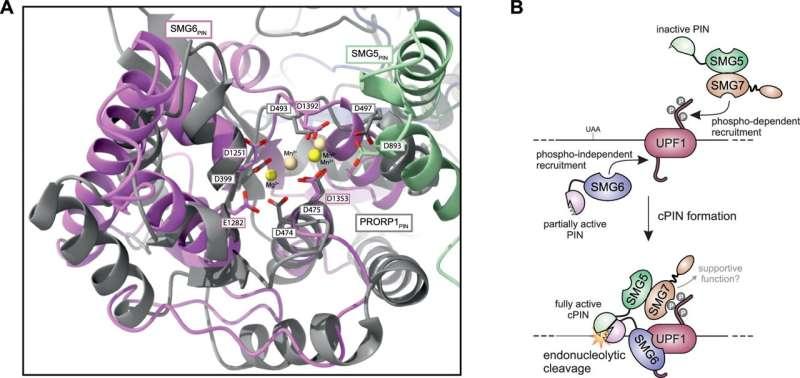
科隆大学遗传学研究所Niels Gehring教授团队与马丁斯里德马克斯·普朗克生物化学研究所Elena Conti教授团队合作,证明SMG5与SMG6蛋白可直接相互作用,并共同形成一种核酸内切酶复合体,从而作为分子“剪刀”对RNA进行定点切割。相关论文以《复合SMG5-SMG6 PIN结构域形成对NMD至关重要》为题,发表在《自然通讯》上。
研究指出,SMG6单独存在时仅表现出较弱的核酸内切酶活性,而SMG5本身不具备切割活性;只有当两者结合后,才会产生完全活跃的酶活性。Gehring表示,研究界约20年前已掌握该机制的组成要素,但一直不清楚这些要素如何组装并发挥作用;通过与马克斯·普朗克生物化学研究所的合作,团队得以补全这一关键环节。
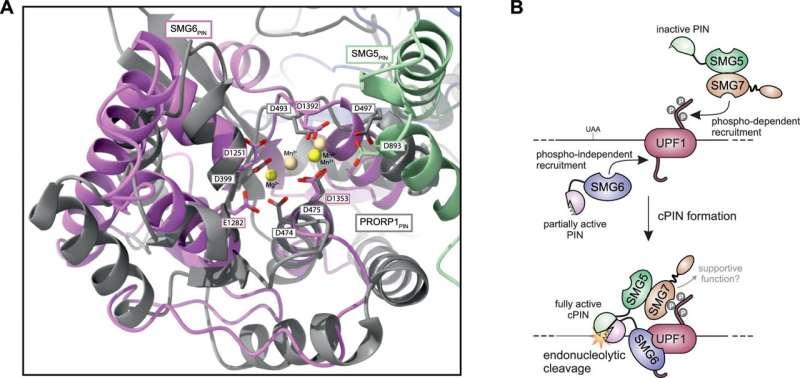
该研究第一作者之一Sophie Theunissen称,两种单独效率不高的蛋白结合后出现显著活性增强,形成“超活性”核酸酶。作者之一Volker Böhm则强调,NMD活性需要在时间与空间上实现高度精确的调控;若核酸内切酶持续处于完全活跃状态,可能对正常mRNA造成附带损害,而由两种独立蛋白通过复杂方式激活的机制,可能体现了系统的安全控制。
研究团队表示,这一发现为早期观察提供了结构层面的解释,并为理解人类细胞中的分子质量控制机制提供基础性进展。鉴于NMD系统的变化与多种疾病相关,该成果也可能为后续生物医学研究提供重要基础。











