早期哺乳动物祖先普遍为夜行性,在恐龙主宰陆地时期多于白天休息。但在演化过程中,包括人类祖先在内的部分哺乳动物谱系曾独立转向昼行性。近日发表于《科学》的一项研究提出,这一转变的线索可能来自基因层面,并指向细胞对环境信号的响应差异。
研究人员指出,昼行性与夜行性物种的大脑主控昼夜节律“时钟”在工作方式上相似,使得“为何会出现相反的活动时间”长期难以解释。新研究将关注点从神经连接转向单个细胞,认为关键差异在于细胞如何感知并响应其微环境中的日常信号。
研究称,在每个24小时周期内,体温、体液平衡等内部条件的细微波动会影响细胞内化学反应,并进一步调节蛋白质合成与修饰等基础过程。这些过程被认为与细胞对“白天或黑夜”的时间预期相关。
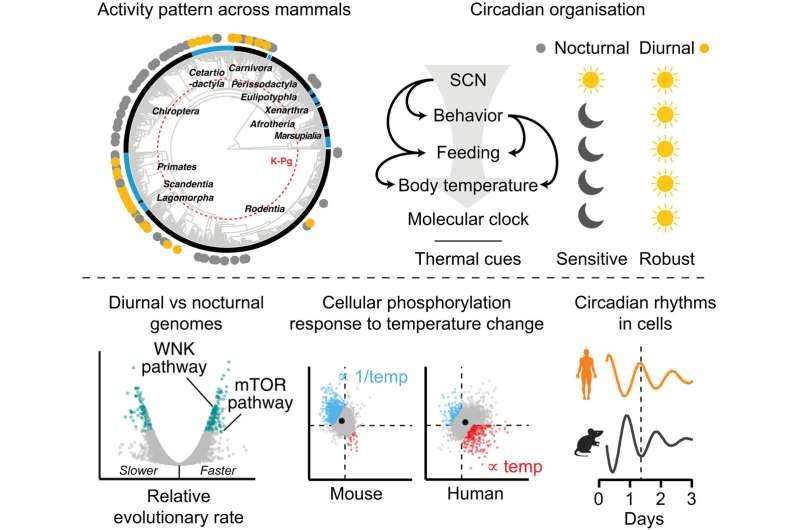
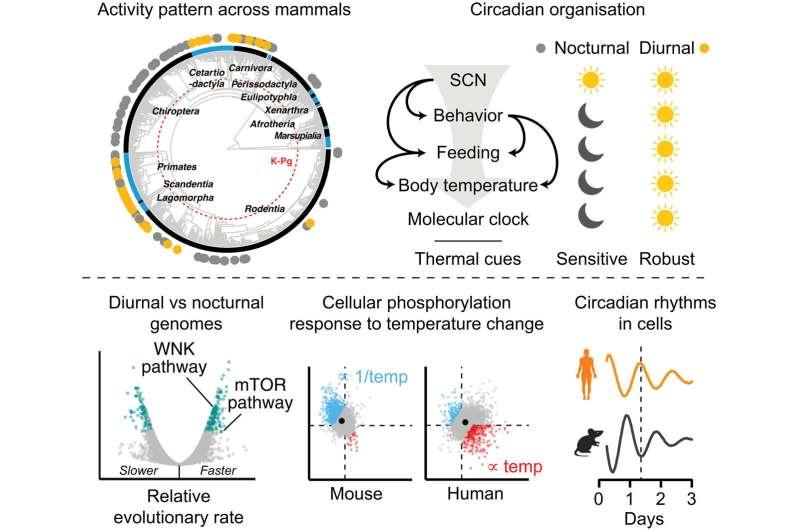
由医学研究理事会(MRC)分子生物学实验室的安德鲁·比尔(Andrew Beale)和约翰·奥尼尔(John O’Neill)领导的团队,对昼行性哺乳动物(包括人类)与夜行性哺乳动物(如小鼠)的细胞进行了比较。研究发现,在暴露于日常温度周期时,昼行性与夜行性哺乳动物细胞的内部昼夜节律时钟会朝相反方向移动,这一差异与各自的自然活动模式相一致。
研究进一步将这种相反反应与两条主要细胞信号通路联系起来:雷帕霉素靶蛋白复合体(mTOR)与无赖氨酸激酶(WNK)。研究人员表示,这两条通路与细胞对营养状态的感知及基础生化反应调控有关。温度变化会引发人类与小鼠细胞在蛋白质合成与活性方面出现不同甚至相反的变化,提示其mTOR与WNK通路对温度等信号的敏感性存在差异。
在瑞典乌普萨拉大学生命科学实验室的马修·克里斯马斯(Matthew Christmas)协助下,研究团队还分析了多个物种的遗传数据。结果显示,mTOR与WNK网络中的相关基因在昼行性哺乳动物中呈现异常加快的进化速度。研究据此认为,从夜间活动向白天活动的转变,可能需要在基因层面对基础细胞功能进行演化调节。
为检验细胞通路变化与活动时间之间的关系,研究团队通过饮食干预对夜行性小鼠的mTOR活性进行轻微调节。研究称,当mTOR功能降低时,小鼠的活跃时间出现向白天转移的趋势,表现得更接近昼行性动物。研究人员据此提出,相关细胞通路可能在一定程度上发挥“昼夜开关”的作用。
奥尼尔表示,理解人类为何为昼行性而许多其他哺乳动物并非如此,有助于从新的角度认识昼夜节律这一与长期健康密切相关的生物学机制;研究也显示,不同物种在感知并响应每日环境节律的机制上存在此前未充分认识的差异。
研究还提及,相关发现提示气候变化可能影响哺乳动物行为。比尔指出,随着大气变暖,外部环境与食物供应之间既有关系正在快速改变,部分哺乳动物可能因此调整活动时间,这可能对生态系统带来广泛影响。











