一项发表于《细胞生物学杂志》的研究披露,致病性最强的疟疾寄生虫之一——恶性疟原虫(Plasmodium falciparum)在人体红细胞内繁殖时,存在一个持续约一小时的关键“冠状”阶段。研究认为,该阶段在寄生虫分裂前发挥类似检查点的作用,帮助其将关键细胞器准确分配至子代,从而维持后续世代的存活与扩增。
疟疾仍是全球破坏性较强的传染病之一,每年造成数十万人死亡,其中多数为撒哈拉以南非洲的幼儿。
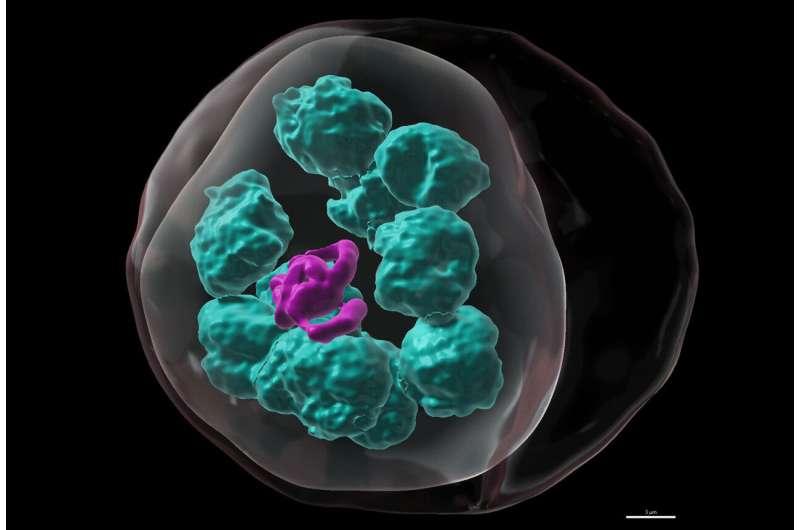
研究由希伯来大学医学院感染与热带疾病研究库文中心及微生物与分子遗传学系的Anat Florentin博士团队主导,聚焦寄生虫细胞内一种名为顶体体(apicoplast)的微小细胞器。研究指出,人类细胞不具备顶体体,但疟原虫依赖该结构生存。顶体体源自光合作用祖先,现被视为寄生虫体内的“微型化学工厂”,可合成寄生虫在红细胞内生长所需的必需分子,包括脂肪酸和异戊二烯类。
为在寄生虫生长过程中追踪其内部变化,研究团队建立了活体成像系统,以高分辨率连续观察寄生虫完整48小时生命周期内的亚细胞结构动态。基于实时追踪核DNA复制与顶体体发育过程,研究人员将顶体体发育划分为四个阶段:伸长、分支、冠状和分裂。
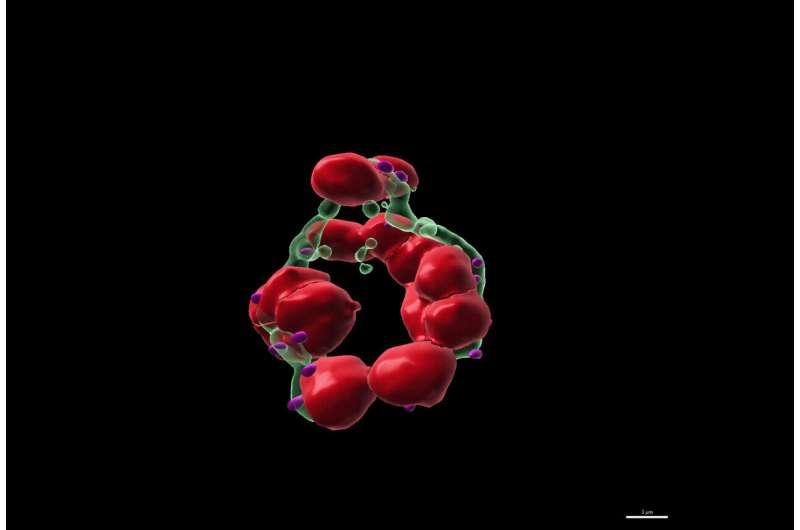
研究强调,“冠状”阶段发生在寄生虫分裂前,持续时间短暂但作用关键。在这一阶段,顶体体跨越多个细胞核,并与一种称为中心粒斑的结构建立连接。研究将该连接描述为一种分配检查点机制,用以确保寄生虫分裂时,每个子细胞都能获得完整且功能正常的顶体体。
在机制验证方面,研究人员通过药物干预阻断不同复制步骤,观察顶体体发育的响应差异。其一,使用阿菲地辛(aphidicolin)抑制核DNA复制后,顶体体发育几乎立即停止,提示顶体体的正常生长依赖寄生虫进入核DNA复制阶段。其二,使用环丙沙星(ciprofloxacin,CIP)抑制顶体体自身DNA复制时,顶体体仍可继续生长并形成分支,但无法形成“冠状”结构。
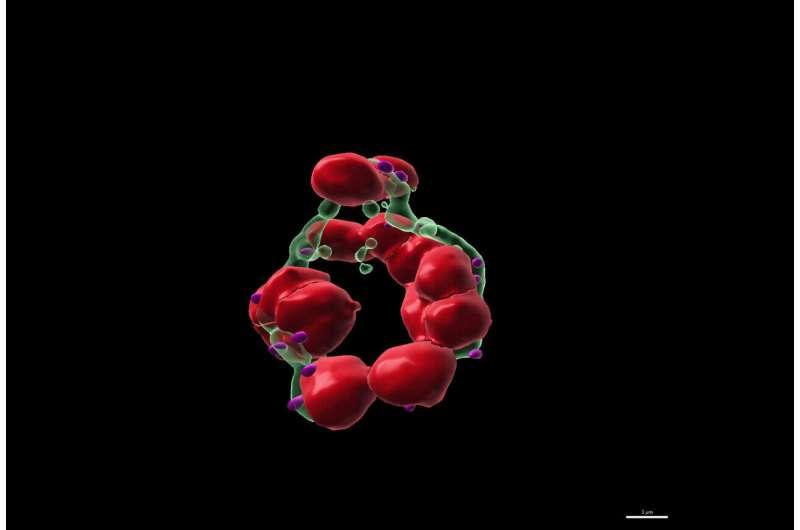
研究进一步指出,当“冠状”阶段缺失时,顶体体无法附着于中心粒斑,导致部分子细胞缺失顶体体,并出现所谓“延迟死亡”现象:第一代寄生虫可能仍能存活,但下一代因缺少顶体体而无法合成必需分子,最终无法存活。
Florentin表示,通过实时追踪DNA复制与顶体体发育,团队观察到核内信号与细胞器内在提示共同参与调控;若能打断核与顶体体之间的通讯,可能阻止寄生虫繁殖。
研究结论认为,顶体体并非在寄生虫内独立运作,其发育与遗传分配依赖寄生虫核内精确的时序信号,尤其与新识别的“冠状”阶段密切相关。研究人员提出,这种依赖关系可能构成潜在脆弱点,未来可考虑以协调寄生虫DNA复制与顶体体发育的信号机制为靶点,干扰寄生虫繁殖过程。











