病毒几乎能够感染地球上所有生物,其关键在于依赖高度特化的蛋白质识别并结合目标细胞表面受体。耶路撒冷希伯来大学农业、食品与环境学院Asaf Levy教授团队近日在《自然通讯》(Nature Communications)发表研究,报告细菌中一类类病毒分子机器相关受体结合蛋白的系统性“目录”,并展示其可能支持对不同细胞类型的靶向能力。
研究由博士研究员Nimrod Nachmias牵头,并与北京国家卫生健康委员会病原体系统生物学重点实验室彭江教授团队合作者王志仁、冯晓共同完成。研究人员称,他们在细菌基因组中发现了一套规模庞大且此前未被系统识别的受体结合蛋白库,其中不少蛋白的结构域来源被追溯至病毒、植物、真菌甚至动物。
聚焦eCIS:由噬菌体尾部演化而来的“注射系统”
该研究的核心对象是细胞外收缩注射系统(eCISs)。研究人员指出,eCIS是一种复杂的类病毒分子机器,起源于噬菌体尾部结构。噬菌体利用尾部结构将遗传物质注入细胞,而在一些细菌中,这类结构被改造为毒素或蛋白质“递送装置”,用于与宿主生物(如昆虫)或其他竞争微生物的相互作用。
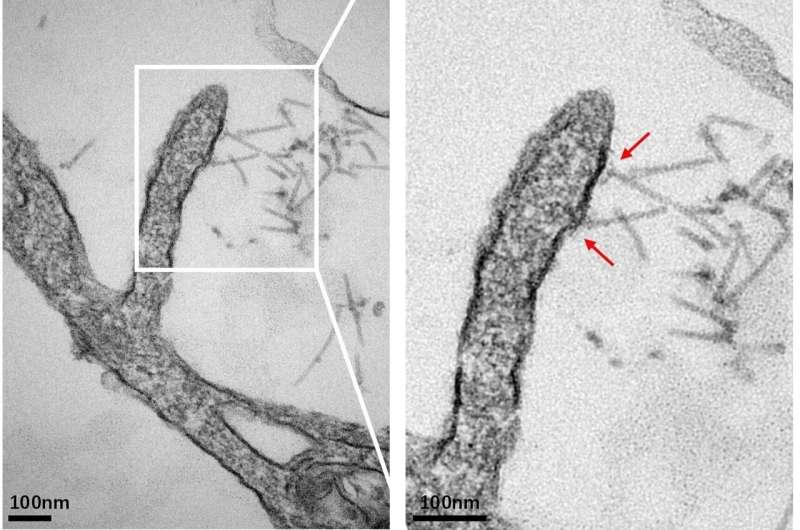
研究团队表示,eCIS外观类似病毒“武器”,但已融入细菌的生态竞争过程;从噬菌体对特定细菌的注入机制,演化为细菌可向多种宿主细胞注入蛋白质的工具,是其关注的关键现象。
新算法识别“难以捕捉”的尾纤蛋白
研究人员长期推测,eCIS需要类似病毒刺突蛋白的受体结合蛋白来识别靶细胞,但相关蛋白难以被传统方法检出。团队解释称,这类被称为尾纤蛋白的受体结合结构域进化速度快、变化大,导致常规基因组搜索策略屡次失效。
为此,研究团队开发了新的计算算法,在大规模基因组数据中定位相关基因。研究结果显示,团队在1,069种细菌和古菌中识别出3,445个尾纤蛋白,这些蛋白编码于2,585个eCIS基因操纵子中。研究人员称,这是迄今最为全面的相关目录之一。
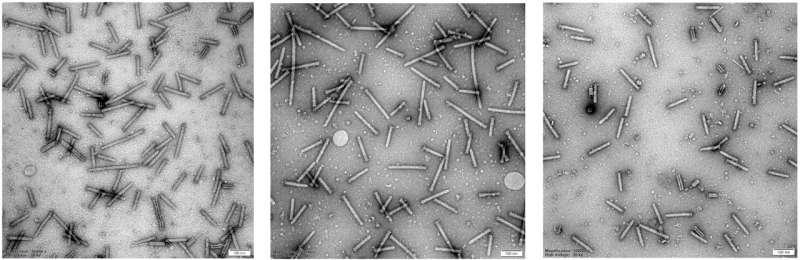
结构域“锚定+可变”组合与水平基因转移线索
研究显示,eCIS尾纤蛋白由两部分组成:一是相对保守的“锚定”结构域,用于将尾纤固定在eCIS颗粒上;二是高度可变的受体结合结构域,决定其可靶向的细胞类型。
借助结构预测工具,团队将这些蛋白归类为1,177个不同的结构域折叠家族,并指出其中不少结构域被预测可与细菌或真核细胞表面的糖类和蛋白质结合。
研究还给出遗传学证据,提示许多结构域可能通过水平基因转移获得,来源不仅包括其他细菌和病毒,也涉及植物、真菌及动物免疫系统成分。研究人员表示,水平基因转移在细菌中并不罕见,但在一个特定基因类别中如此频繁地呈现来自多样化真核生物的来源线索,在自然界较为少见。
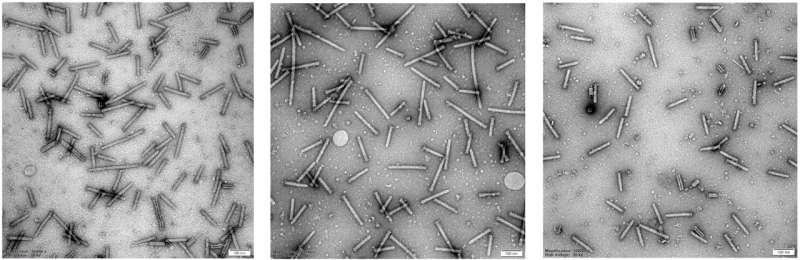
实验验证:候选尾纤可介导对人类细胞的特异递送
为检验上述发现的功能意义,研究人员选取了一个来自Paenibacillus eCIS的候选尾纤蛋白。该蛋白与血凝素相似,后者是流感和麻疹病毒中已知的受体结合蛋白。基于这一相似性,团队提出该候选蛋白可能与人类细胞结合。
研究人员随后构建了携带该尾纤的嵌合eCIS颗粒。实验结果显示,该颗粒能够结合并向人类THP-1单核细胞样细胞注入蛋白质,而对其他细胞类型未观察到相同效应。
进一步实验提示,人类细胞表面的D-甘露糖可能是关键受体之一:外加D-甘露糖可对结合产生部分阻断作用。研究团队还报告,电子显微镜图像捕捉到类病毒颗粒在向人类细胞递送分子货物前的附着瞬间。
工程化应用与基础问题并行
研究团队表示,除其团队外,包括多家初创企业在内的其他研究力量也在探索工程化eCIS系统。研究人员认为,此次识别出的数千种自然进化的受体结合蛋白,为未来将药物、酶或其他治疗分子精准递送至特定细胞类型提供了更大的候选工具箱。
同时,研究也提出一系列基础生物学问题。研究人员指出,许多eCIS系统在自然环境中的具体功能仍不清楚,包括其靶向哪些细胞、在何种条件下被激活等;而本次建立的尾纤蛋白目录为后续研究提供了可用于系统探索的“地图”。











