抗生素曾将多种致命细菌感染转变为可控疾病,但在抗生素耐药性上升的背景下,部分在实验室条件下表现有效的药物在真实感染中却常出现疗效不足。加州理工学院与普林斯顿大学研究人员近期通过模拟更接近人体内环境的细菌群体结构,提出一种可能的解释:微生物可获得的营养水平会显著影响抗生素的杀菌过程。
研究团队在《自然通讯》发表论文,报告其在空间结构化细菌群体中观察到的“死亡前线”现象。加州理工学院化学工程、生物工程及生物物理学教授Sujit Datta表示,实验显示细胞并非在抗生素作用下均匀死亡,而是出现逐步推进的杀灭过程:代谢更活跃、位于群体表层的细胞先被杀死,而处于营养匮乏状态的内部细胞更可能存活。论文第一作者为Datta团队博士后Anna Hancock。
在传统药敏测试中,研究人员通常在充分混合的液体培养基中培养细菌,并加入不同浓度抗生素,依据细菌何时停止生长来确定最低抑菌浓度(MIC)。Datta指出,这类方法隐含的推断是提高抗生素浓度即可杀死细菌,但在真实生物体内,细菌群体往往呈现空间结构化、非混合的状态,药物与营养的分布并不均匀。
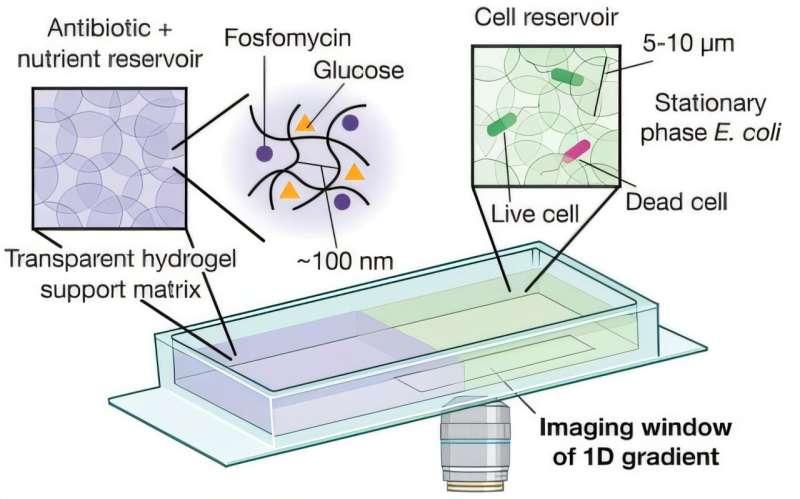
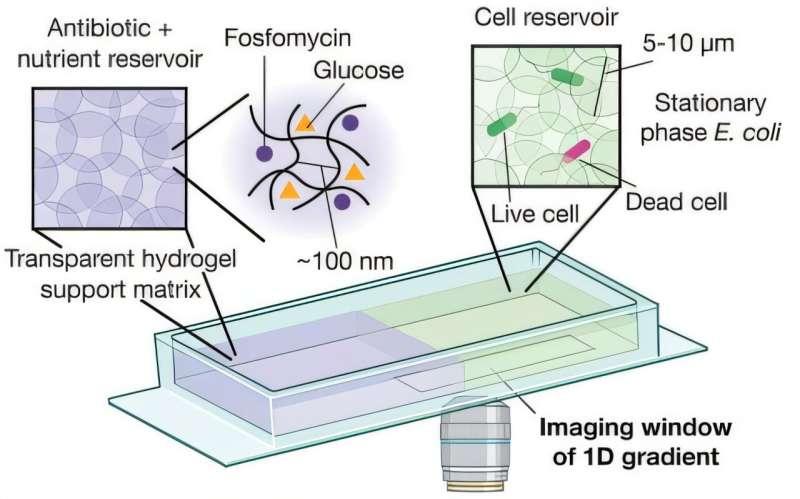
为更贴近体内情形,研究团队构建了基于凝胶的感染模型:培养皿一侧为含细菌的、类似细胞外基质的凝胶,另一侧为不含细胞的同类凝胶,用以模拟外部环境,两侧由隔板分隔。实验中,研究人员在无细胞一侧加入待测抗生素及细菌所需营养物,随后移开隔板,使抗生素与营养物扩散进入含菌区域,并通过光学显微镜监测细胞荧光信号以判断生死。
实验结果显示,在无营养条件下,即便加入高浓度抗生素,细菌群体也几乎不受影响;而在加入营养物后,群体中会出现一波由外向内推进的死亡浪潮。Datta将其描述为“扫荡式”的死亡过程,提示营养供给与消耗在抗生素杀菌中起关键作用。
研究还观察到营养供给的“双刃剑”效应:增加营养可增强杀菌效果,但当营养过量时,部分在死亡前线后存活的细胞可能继续生长,形成耐药亚群。Datta表示,微生物群体具有异质性,不同细胞对抗生素的敏感度并不一致,这使得在大量细胞被杀死后仍可能残留存活者,而营养过剩会为其再生长提供条件。
除实验外,团队还提出一个数学模型,用以刻画营养物扩散进入群体、激活细胞代谢并使其成为抗生素作用靶标的动态过程。Datta称,该模型能够再现实验观察,并用于估计在不同剂量下抗生素的杀灭程度、速度以及所需营养量。
研究团队表示,这一发现未必会立即带来新型抗生素,但为评估哪些抗生素更可能在人体内发挥作用、以及以不同方式研究抗生素耐药性提供了新的起点,并为进一步探讨如何避免耐药再生长等问题奠定基础。











