北卡罗来纳大学医学院研究人员报告称,免疫系统中的一种先天免疫蛋白可能在特定条件下削弱β-内酰胺类抗生素的杀菌作用,使细菌在并未产生传统意义“抗药性”的情况下仍能存活。相关研究发表于《美国国家科学院院刊》(PNAS)。
β-内酰胺类抗生素包括阿莫西林、青霉素等,临床上常用于治疗链球菌性咽喉炎、耳部感染,以及尿路感染、肺炎和败血症等多种细菌感染。研究团队指出,即便细菌不具备抗药性,这一类药物也可能出现治疗失败。
该研究通讯作者、北卡罗来纳大学医学院微生物学与免疫学副教授Brian Conlon表示,团队发现一种关键的先天免疫蛋白会通过隔离必需金属,意外地帮助细菌在最常用的抗生素类别之一中存活;这被其描述为β-内酰胺类抗生素与免疫系统之间“不幸的拮抗作用”,可能导致临床治疗失败。
研究人员在论文中讨论了“抗生素耐受性”的风险:在严重或反复感染中,细菌可在较长时间内承受抗生素的杀灭作用。研究提到,约20%的接受氧氟沙星治疗的甲氧西林敏感金黄色葡萄球菌(MSSA)感染患者死亡,这一结果与抗生素耐受性相关。
为解释常用抗生素为何会出现耐受性,Conlon团队将研究重点放在宿主免疫因素对药物作用的影响上。研究人员介绍,β-内酰胺类抗生素主要通过破坏细菌细胞壁发挥作用;细胞壁受损后,细菌酶类自溶素会进一步分解细胞壁,导致细胞破裂并杀死细菌群落。
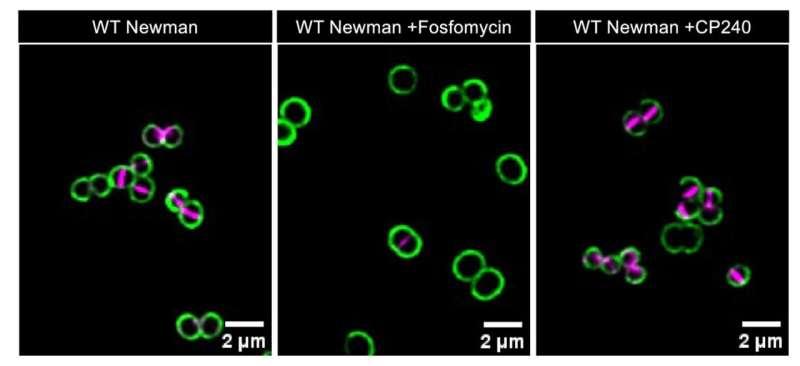
在医学博士/博士候选人Amanda Z. Velez带领下,团队聚焦于钙保护素(calprotectin)这一在感染部位发挥“第一响应者”作用的免疫蛋白,并建立金黄色葡萄球菌模型评估其对抗生素活性的影响。研究发现,钙保护素通过剥夺细菌所需的锌和锰,能够抑制葡萄球菌的生存与生长。但当研究人员将含钙保护素的细胞模型暴露于头孢唑林时,观察到抗生素不再有效杀死细菌。
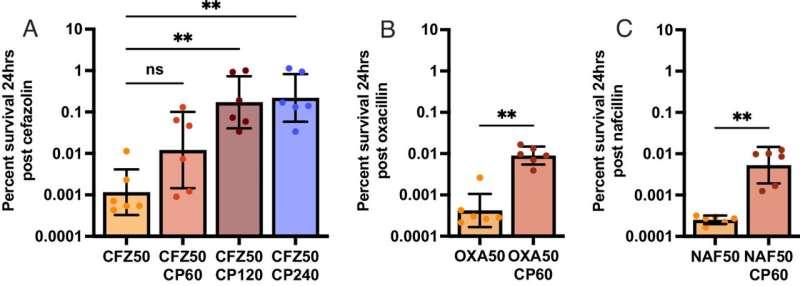
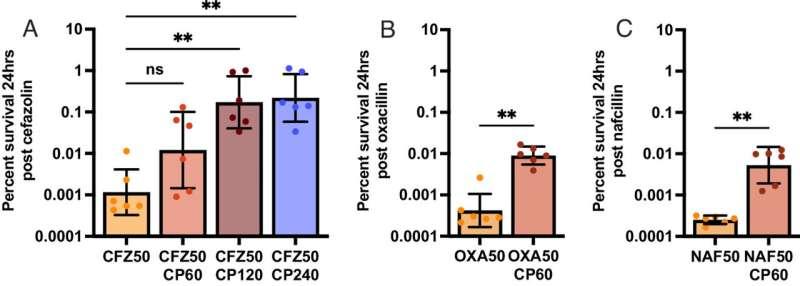
进一步实验显示,钙保护素在夺走锌的同时,也带走了自溶素有效降解细胞壁所需的金属辅因子,从而阻断了β-内酰胺类抗生素依赖的关键杀菌环节。研究人员还在小鼠模型中验证了这一机制:在不产生钙保护素的小鼠中,氧氟沙星的疗效显著增强。
研究团队表示,这些结果提示抗生素耐受性并非仅由病原体自身决定,宿主免疫系统也可能成为影响因素。论文称,团队正在研究可降低钙保护素水平和/或提高患者锌水平的药物候选物,以期帮助抗生素更有效地控制感染。Velez表示,这些效应揭示了抗生素敏感性中一个尚未充分探索的维度,可能成为改善治疗效果的潜在靶点。
研究人员还计划将相关观察扩展至其他需要锌参与自溶活性的细菌,包括难辨梭状芽胞杆菌、肺炎链球菌、幽门螺杆菌和大肠杆菌,以评估其是否也会因钙保护素而出现耐受性。











