多年来,细胞内蛋白质cereblon(CRBN)作为关键组成部分,支撑了多款价值数十亿美元的抗癌药物机制。最新研究显示,除既有认识外,cereblon还可通过不同结合位点的协同作用,影响哪些蛋白质被标记并送入细胞降解系统。
《自然》杂志近日发表的一项研究称,研究团队首次鉴定并绘制了cereblon上的变构位点(allosteric site)——一个此前未被系统刻画的隐藏结合口袋。该研究由化学与化学生物学教授Christina Woo团队牵头,并与葛兰素史克(GSK)以及斯克里普斯研究所的科学家合作完成。
cereblon是一个蛋白复合体的一部分,负责对其他蛋白进行标记以便销毁。该蛋白因与沙利度胺(thallidomide)相关而广为人知:沙利度胺在20世纪50至60年代曾用于治疗孕吐,但随后被证实会导致出生缺陷。数十年后,沙利度胺及相关化合物被重新用于治疗血液癌症,原因在于它们能够重新引导cereblon去标记特定致病蛋白,从而触发降解。
上述机制与“靶向蛋白降解”策略相关:研究人员通过设计小分子,将目标蛋白带到cereblon附近,由cereblon完成标记并交由细胞降解机制处理。
发现第二个结合口袋
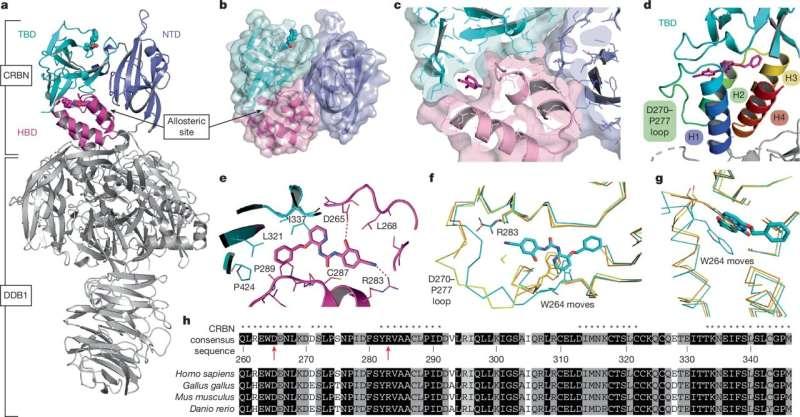
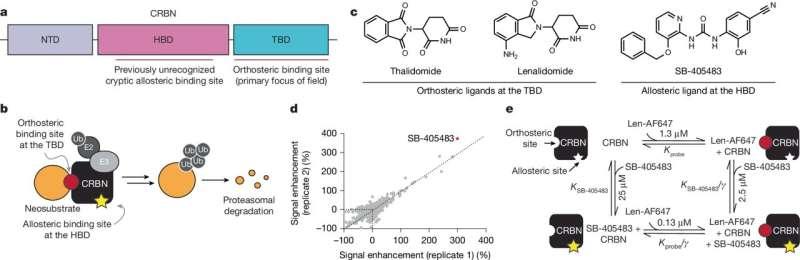
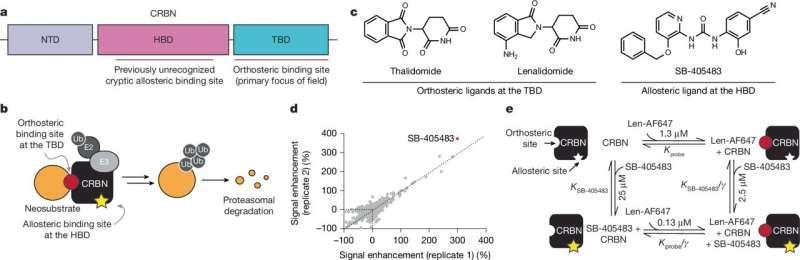
研究称,过去相关研究主要聚焦于cereblon的正构结合位点(orthosteric site),即沙利度胺结合的同一位点。此次工作则指出,cereblon还存在第二个口袋——变构位点。该位点并不取代主结合位点,而是在主位点被激活后改变后续反应过程。
研究团队披露,GSK科学家最初发现一款小分子SB-405483,其信号增强效应提示其可能与cereblon的另一位置结合。GSK执行董事、哈佛大学前美国癌症协会博士后Andrew Benowitz表示,团队据此判断变构结合剂可能打开对cereblon生物学的新理解,并与Woo团队合作推进验证。

细胞实验显示可“增强”也可“保护”
Woo团队随后开展细胞实验,使用报告细胞系生成不同的cereblon新底物(可被降解的蛋白质)并融合荧光标签;当目标蛋白被降解时,荧光信号减弱。研究人员在主位点使用标准cereblon靶向药物,并在有无变构配体条件下处理细胞,以观察第二个位点对蛋白降解的影响。
研究结果显示,在不同组合条件下,变构配体对降解的影响并不一致:在某些组合中可使部分目标更易被降解;在另一些组合中则表现为保护作用,降低降解程度。研究称,许多情况下效果取决于与之搭配的正构结合药物。
第一作者、Kenneth C. Griffin研究生院研究生Vanessa Dippon表示,调节变构位点既可能增强特定新底物的降解,也可能抑制降解,从而改变cereblon对新底物降解的谱系与格局。Woo则指出,该选择性带来的直接应用设想之一,是在增强正构配体对目标效力的同时,减少对非目标蛋白的招募,以降低脱靶毒性。
冷冻电镜结构解释作用机制
为解释隐藏位点为何能带来广泛影响,团队进一步与斯克里普斯研究所冷冻电镜专家Gabriel Lander合作,获得cereblon不同构象的高分辨率结构。
研究称,当主位点与变构位点同时被占据时,cereblon会经历一个此前未见的中间构象,并最终形成更封闭的形态;该形态更有利于捕获被标记销毁的蛋白。结构结果还显示,变构配体会轻微推动主位点药物的位置变化,为细胞实验中观察到的降解模式差异提供了结构层面的解释。
潜在药物开发方向
研究认为,这一发现带来多种后续路径:其一,将变构配体作为现有cereblon相关癌症药物的辅助调节剂,以增强对目标蛋白的作用并限制与副作用相关蛋白的降解;其二,围绕变构口袋设计新型分子胶或双头降解剂分子。
Woo还表示,该工作也为理解细胞如何自然调控cereblon及相关酶提供线索,并提出体内可能存在执行类似调控功能的内源性小分子,但相关认识仍处于起步阶段。
本文由哈佛大学官方报纸《哈佛公报》授权发布。更多大学新闻,请访问Harvard.edu。











