罗格斯大学纽瓦克分校科学家开发出一种基于RNA的纳米技术平台,可在活体人类细胞内生成并自组装成预设结构,并通过编程方式干预有害细胞扩散。相关研究近日发表于《自然通讯》。研究团队表示,已开始在人体细胞培养体系中验证该平台,并正进一步将其用于人类癌细胞测试,作为潜在癌症治疗方案的探索方向,但目前尚未完成研究或披露结果。
该平台被研究人员定位为可用于生物医学研究与治疗的分子工具。团队称,其优势在于结构与功能可定制,具备同时指向多种有害基因与蛋白质的潜在多功能性。
这项工作由罗格斯大学纽瓦克分校化学系张飞教授与生物科学系让-皮埃尔·埃切加雷教授牵头,联合跨学科团队完成。张飞表示,团队提出了一种“具有可编程功能的人造RNA结构”的新设计策略。
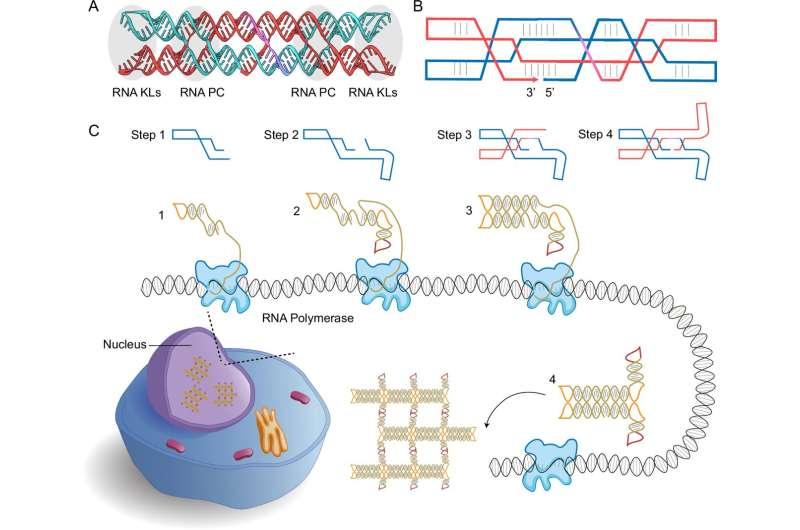
研究人员介绍,该技术思路建立在细胞依赖DNA指令运行的基础上:RNA作为信使分子,携带信息指导细胞合成蛋白质。与将预制分子直接递送入细胞的路径不同,团队采用向细胞提供合成DNA模板的方式,使细胞内部产生特定RNA片段,并在细胞内折叠、自组装为精确形状,同时实现可控定位。组装后的RNA结构可携带功能域,并可根据不同生物医学用途进行重新编程。
团队将这些RNA片段比作“微型乐高积木”,强调其在细胞内自动寻找并拼接的特性,并称该结构可被重新设计为不同几何形态以承载不同功能。
埃切加雷指出,这类能力对癌症研究具有意义,因为癌症往往由多种功能失调基因共同驱动。团队的目标之一,是通过定制RNA结构识别疾病特异信号,从而影响癌细胞而尽量避免损伤健康细胞。研究人员已开始尝试利用该平台禁用癌症干细胞,以阻止其增殖。埃切加雷表示,团队正在尝试靶向癌基因,评估是否能够禁用被认为与癌症起始和扩散相关、且具有治疗抵抗性的癌症干细胞。
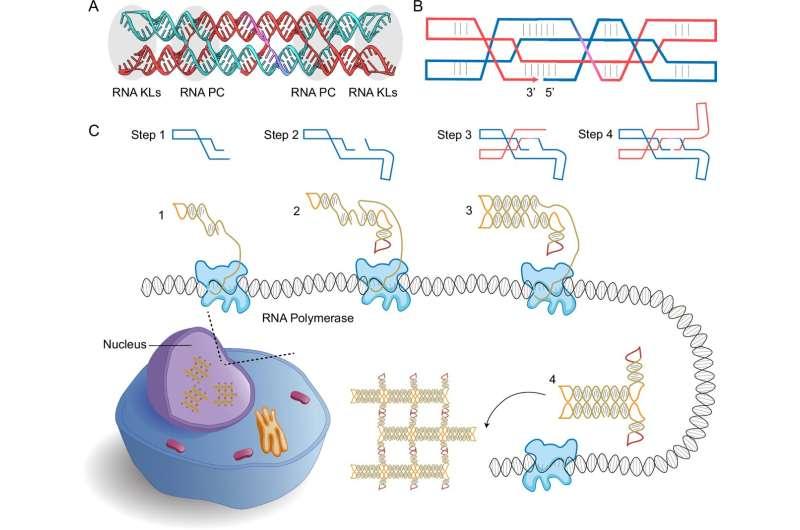
研究团队同时指出,目前多数RNA疗法通常以单一分子为靶点,而该平台被设计为可编程与多个靶点同时交互。此外,该平台也被描述为可与现有RNA疗法配合使用,研究人员称可将传统RNA疗法中的片段与功能序列整合进该平台以增强效果。
在产业化进展方面,团队表示已获得临时专利批准,并正在寻求投资者、产业合作伙伴与研究伙伴,以推动后续研发进程,包括临床试验。研究人员还称,除癌症外,该纳米技术也可被定制用于靶向由基因与蛋白质异常表达驱动的其他疾病。











