气泡囊被认为是目前已知体量最大的蛋白质纳米结构之一,由微生物在细胞内合成并自组装形成。该结构呈空心、充满空气的圆柱形,存在于部分水生微生物中。由于其能够反射声波,气泡囊近年来被研究人员关注,相关特性被视为可用于新型诊断与治疗工具的潜在基础。不过,在实验室条件下让非天然宿主细胞稳定生产气泡囊一直较为困难,成为限制其应用推进的因素之一。
《自然通讯》近期发表的一项研究中,莱斯大学生物工程师乔治·卢(George Lu)领导的团队报告称,他们开发了一套新的基因调控系统,用于改善气泡囊生产过程中宿主细胞的存活状况。卢表示,气泡囊反射声波的能力使其在生物医学研究与临床应用中具备作为声学报告系统的潜力,但在实际应用推进上仍面临生产端的挑战。
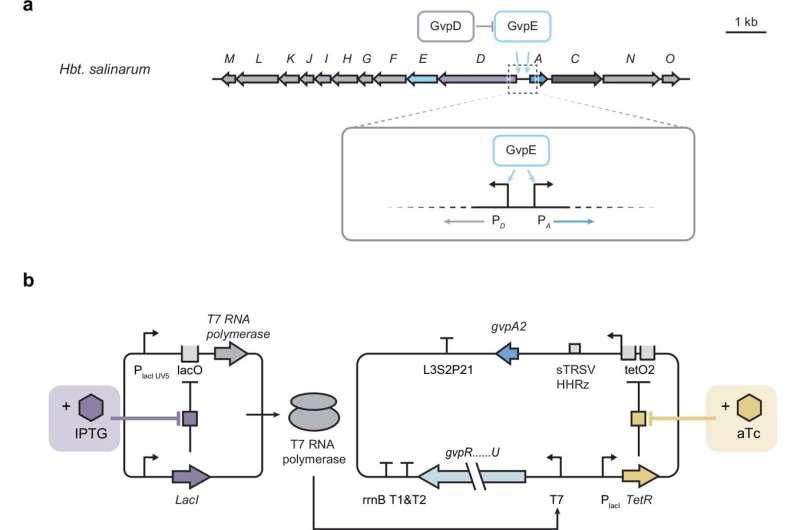
研究团队指出,在大肠杆菌等非天然细菌宿主中表达形成气泡囊外壳所需的10个基因,会给细胞带来显著压力,甚至导致细胞死亡。为降低这种负担并维持宿主细胞健康,团队设计了一个两阶段、双诱导剂系统,以更精确地控制不同蛋白质的表达时序与表达量。
卢团队进一步报告称,在该复杂多组分系统中,若多种蛋白质同时生产并组装,细胞压力往往上升。通过调整表达顺序,先启动组装因子的表达、再生产主要外壳蛋白,可减少通常由同步表达引发的毒性。论文作者之一、卢实验室博士后研究员李宗儒表示,在诱导外壳蛋白之前,让组装因子提前表达两到三小时,有助于确保构建结构所需的细胞“机械装置”先行就绪。
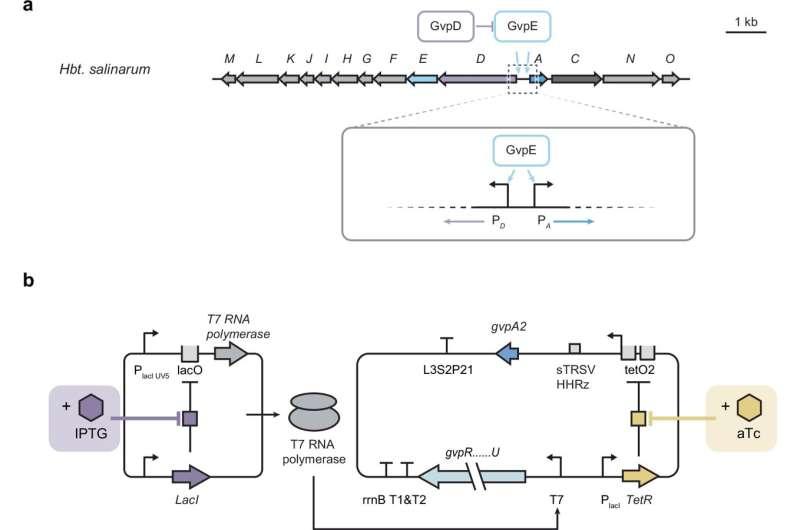
卢表示,通过将“同时生产”改为“顺序生产”,该基因调控系统把原本更易出现混乱的组装过程转变为更有序的生产流程,结果是宿主生物更健康、气泡囊产量更高。研究团队认为,这一方法为临床与科研场景提供了更稳健可靠的气泡囊生产手段,并可能适用于其他多组分蛋白质复合物的生产。
发表评论
登录后才可评论。
去登录











