达姆施塔特工业大学合成生物学中心两个工作组组成的跨学科团队报告称,他们开发出首个基于RNA的遗传开关,可在活细胞中精确复现数字电路关键模块之一——NAND门的逻辑行为。相关研究已发表在《核酸研究》(Nucleic Acids Research)。
该团队介绍,这类“数字RNA开关”建立在核糖开关(riboswitch)机制之上:特定RNA序列能够对小分子配体产生响应。作为mRNA的一部分,核糖开关可调控mRNA向蛋白质的翻译过程;当配体结合后,RNA构象发生变化,从而对核糖体形成阻碍并影响蛋白质合成。
研究人员指出,核糖开关的优势在于无需额外蛋白质即可发挥作用,序列长度通常少于100个核苷酸,能量消耗低,对细胞代谢负担较小,因此被视为合成基因调控的工具之一。
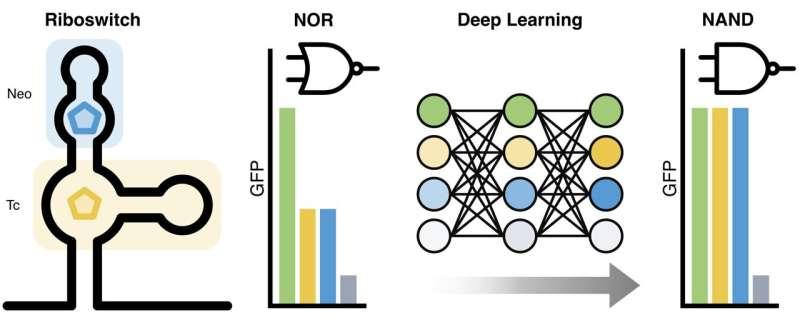
达姆施塔特工业大学合成生物学中心研究员Daniel Kelvin表示,团队通过将两个核糖开关进行无缝连接,构建出具备两个不同输入的遗传开关元件,并在活细胞中实现类似计算机逻辑的功能。该系统由两个核糖开关组合而成,其输出行为对应布尔逻辑中的NAND门。
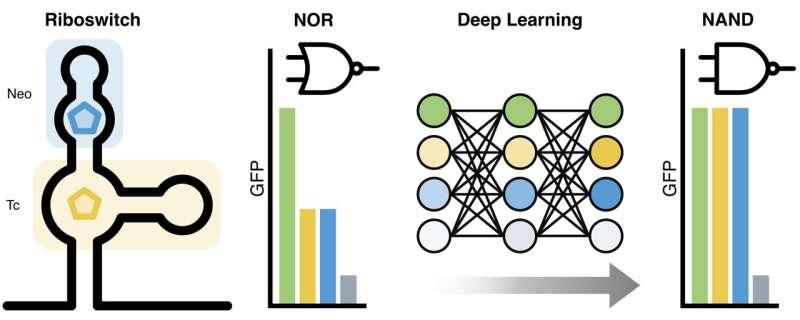
在数字技术中,NAND门仅在两个输入均为“开”时输出“关”,其余情况下输出为“开”。对应到该生物系统中,只有当两个配体同时结合到核糖开关时,基因表达才会被关闭;若缺少任一配体,基因表达保持活跃。研究团队称,这种复杂行为尚未在自然界中观察到,同时由于序列变体数量会随序列长度呈指数增长,构建混合NAND核糖开关具有较高难度。
为实现该目标,研究团队将高通量实验筛选与贝叶斯优化等机器学习方法结合,借助计算机模型对NAND门进行重新设计。研究首先构建了一个呈现部分NAND特征的混合核糖开关,并据此生成RNA变体库。随后,团队制备了数千种混合核糖开关变体,重点在连接两个结合口袋的中央“通信模块”区域进行变体设计,并通过流式细胞术测试其在不同配体组合下的表现,以获得精确测量数据。
合成生物学中心研究员Erik Kubaczka表示,团队随后使用深度学习模型预测哪些RNA变体更接近NAND功能,并通过基于贝叶斯优化的算法有针对性地选择新的候选变体,使模型在每轮实验后持续学习。
研究还强调了并行化实验设计的重要性。为同时提出多个核糖开关变体以提升实验效率,团队在原本顺序进行的贝叶斯优化流程中引入Kriging Believer方法。该方法在提出建议后无需等待实验数据返回,而是将当前模型预测纳入训练,并在已选变体的上下文中选择下一批候选序列,以避免挑选过于相似的序列,从而支持模型有效学习。
研究结果显示,在仅测试82个变体后,系统即筛选出多个高度优化的核糖开关。其中表现最佳的候选者呈现出接近数字化的NAND功能,在“开”与“关”状态之间具有清晰区分。
研究团队认为,功能稳定的NAND核糖开关具有里程碑意义,因为包括AND、OR、XOR等在内的多种逻辑功能均可由NAND门构建。研究人员指出,这为在活细胞中实现逻辑决策提供了新的可能性,例如仅在特定营养物或信号分子组合存在时才触发某种产物的生成。
研究还提到,该类系统可用于构建面向医学与环境的生物传感器,例如检测特定代谢状态、识别肿瘤特征,或仅在特定组合条件下报告环境毒素。
据介绍,该项目由达姆施塔特工业大学Beatrix Süß教授(合成生物学中心合成RNA生物学组)与Heinz Koeppl教授(合成生物学中心自组织系统组)领导。团队表示,新型混合核糖开关与基于机器学习的设计流程可为遗传电路构建提供加速平台,并展示了生物学与机器学习方法结合在开发新型功能RNA元件方面的应用路径。











