细胞在面临生存或死亡等关键抉择时并非“凭直觉”行动,而是遵循一套分子层面的调控规则。长期以来,研究人员多依赖RNA特征或蛋白质产物等间接指标来推断细胞内蛋白质是否处于活跃状态,但难以在蛋白质生成后对其活性进行直接测量。
新方法:在单细胞内直接计数酶的活跃状态
圣福恩·伯纳姆·普雷比斯医学发现研究所与弗罗茨瓦夫科技大学的科学家在《细胞报告》发表研究,提出一种用于测量酶活性的全新方法。研究团队指出,蛋白质的激活状态并不能简单由其产生量推断,这一现象在细胞死亡相关信号研究中尤为关键。
人体内许多细胞会被持续监控,以判断是否需要被清除。功能失调的细胞可能因衰老或突变而被程序性细胞死亡(凋亡)机制移除;而癌症的一个显著特征是癌细胞能够逃避凋亡并持续增殖。
论文资深及共同通讯作者、圣福恩·伯纳姆·普雷比斯名誉教授盖伊·萨尔维森(Guy Salvesen)表示,科学界已界定多条参与凋亡的细胞信号通路,但要更好理解这些信号的作用,需要明确“触发细胞凋亡需要多少活跃的酶分子”。
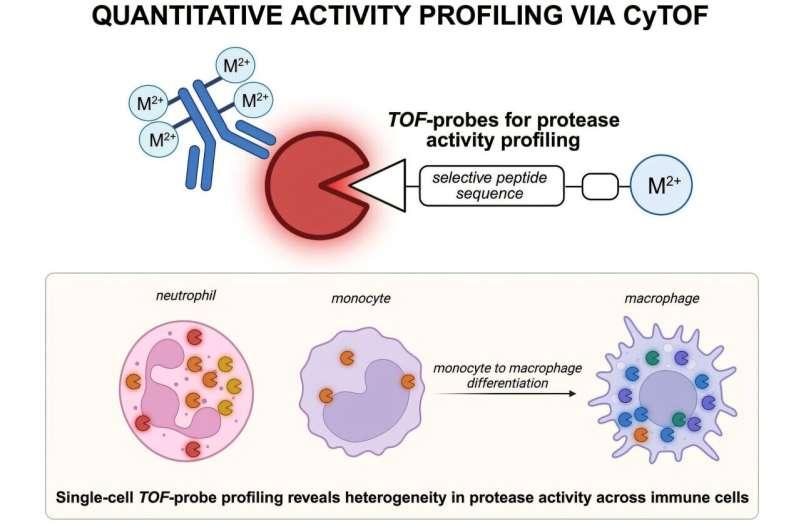
金属标记探针与质谱细胞仪:区分活跃与非活跃蛋白酶
研究团队将目标锁定在蛋白酶(protease)上。这类酶可切割其他蛋白质,参与多种关键细胞功能,其中包括触发程序性细胞死亡。
为实现更直接的追踪,研究人员设计了新的化学探针,可在蛋白酶的活跃或非活跃形式上分别植入不同的金属标记。随后,这些金属标签可通过质谱细胞仪进行分析。该单细胞仪器通过检测金属标签的质量信号,使研究人员能够在单个细胞内精确计数不同状态的酶分子数量。
论文第一及共同通讯作者、圣地亚哥米拉玛学院兼职教师、萨尔维森实验室前轮换学生卡塔日娜(卡西亚)·格罗博兹(Katarzyna “Kasia” Groborz)表示,此前该领域的结论主要基于RNA特征和间接标记,而新技术有助于补足关于死亡细胞分子机制的直接信息,例如哪些酶处于活跃状态、哪些酶影响细胞死亡类型,以及这些因素如何随疾病发生变化。
在免疫细胞中的测试:酶的“产量”与“活性”并不等同
研究人员在从健康献血者分离的两类免疫细胞中测试该方法。在负责抵御感染的白细胞中性粒细胞中,研究发现不同中性粒细胞携带的蛋白酶数量差异显著,且活跃与非活跃酶的比例也各不相同。
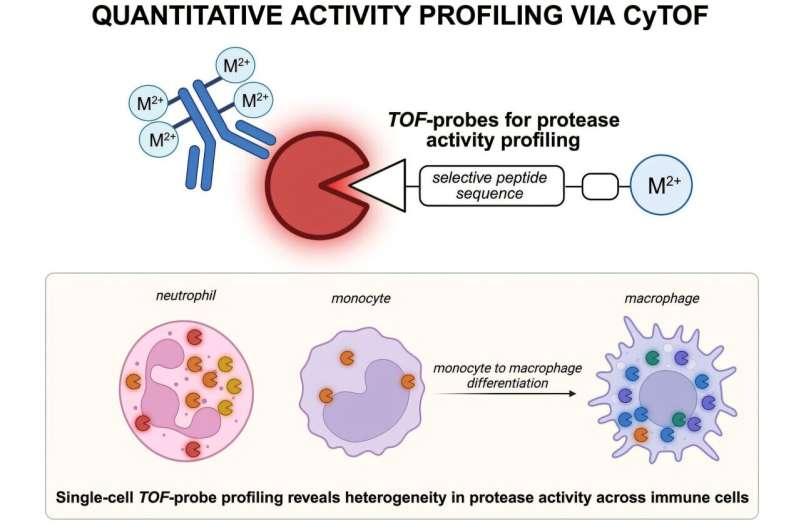
以半胱氨酸蛋白酶为例,即便在表达相关基因较高、产生更多酶分子的免疫细胞中,这些酶也多处于休眠状态。萨尔维森据此表示,数据支持研究团队的结论:蛋白酶活性是在蛋白质产生之后受到调控,这限制了仅凭基因表达所反映的丰度来推断活性的能力。
在另一组实验中,研究人员观察单核细胞向巨噬细胞分化过程中酶活性的变化。该转变有助于细胞对抗癌症或感染,同时伴随蛋白酶产生与活性的动态调整。研究团队称,所观察到的酶水平与活性模式变化与单核细胞和巨噬细胞功能变化相一致:巨噬细胞抑制凋亡相关酶的构建与活性,并优先激活与炎症程序相关的酶,从而促进免疫系统对癌症、感染或损伤的反应。
研究团队:有望绘制更精确的单细胞变化图谱
格罗博兹表示,能够描述这些过程令人振奋,因为研究人员可以开始绘制组织内单个细胞发生变化的更精确“地图”。萨尔维森则称,尽管研究起点是免疫细胞与凋亡,但该方法未来可扩展至其他细胞死亡形式和疾病研究。
研究团队表示,最终希望通过对单个细胞内蛋白质水平变化进行定量刻画,为药物发现提供更清晰的靶点信息,明确需要阻断或激活的对象,以支持更有效的疾病治疗策略开发。











