许多癌症治疗药物具有较强毒性,在体内循环过程中可能损伤健康组织并引发严重副作用。围绕如何将药物的细胞毒性作用尽可能限制在肿瘤部位,雪城大学研究人员近日公布一项化学策略,尝试让药物在抵达癌细胞前保持“休眠”,并在特定位置被触发后再释放活性成分。
雪城大学艺术与科学学院(A&S)化学助理教授胡晓然及其团队在《应用化学国际版》(Angewandte Chemie International Edition)发表研究,提出一种原型“锁与钥匙”系统:将治疗药物以不活跃的“笼”形态封装,只有在遇到另一种化学触发剂时,才在触发环境中快速、选择性地释放药物。研究团队表示,该平台旨在提供一种可用于调控活体系统内化学键“何时、何地断裂”的新方法。
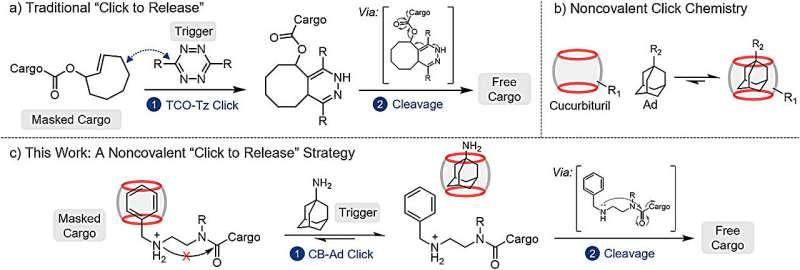
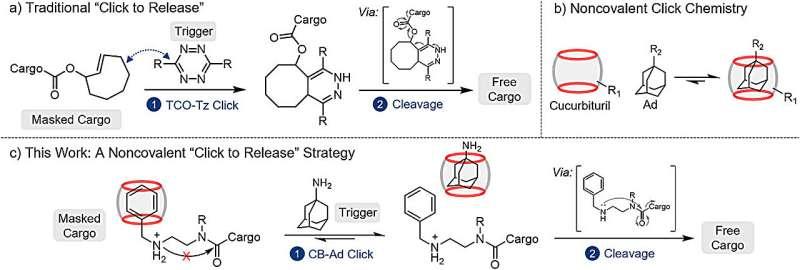
该研究以“生物正交化学”(biorthogonal chemistry)为核心思路,即在高度选择性的条件下进行化学反应,使其能够在细胞或体内等复杂生物环境中发生,同时尽量不干扰原生生物过程,也不易被复杂环境所干扰。研究人员据此将药物分子“笼装”为相对安全的惰性形式,以降低其在非目标部位的毒性暴露;当“笼装”药物与“触发”分子相遇后,二者发生快速且选择性的反应,从而在触发位置释放有毒药物。研究团队指出,如果触发剂被引入特定位置(例如肿瘤部位),则有望实现局部药物释放。
在具体实现上,该平台采用生物正交超分子化学机制,通过“宿主”分子对互补“客体”分子的高选择性识别与结合,在复杂生物环境中形成可靠相互作用,并将其作为释放药物的“钥匙”。胡晓然表示,团队希望开发一种具有广泛适用性的工具,用于调节不同类型治疗药物的活性。
研究团队在细胞实验中对不同癌症治疗剂的释放进行了控制,并调节了对癌细胞的杀伤效果。胡晓然称,该系统的目标是让治疗的细胞毒性作用在需要的时间和地点开启,尽可能将影响限定在癌细胞或肿瘤细胞相关环境中,从而减少对人体其他部位的影响。
不过,研究也指出该策略面临稳定性挑战。团队采用的宿主—客体超分子相互作用在正常体温(37摄氏度;98.6华氏度)下可能减弱,导致药物在到达预定触发环境前出现缓慢“泄漏”,从而影响控制效果并带来潜在安全风险。胡晓然表示,团队将把提升宿主—客体结合强度作为后续重点,以尽量减少在生理温度与pH条件下的过早释放。
研究人员同时提到,该平台的工作原理并不依赖特定生物靶点,因此潜在上不局限于癌症药物,可适配多种治疗方案。团队表示,距离临床应用仍需时间,但该研究为将药物设计为可在特定时间与地点精准开启效应的“可编程系统”提供了新的研究基础。












