新冠疫情推动信使RNA(mRNA)疫苗快速发展。首款新冠mRNA疫苗于2020年12月8日开始接种。数学模型显示,仅在接种后的首年内,mRNA疫苗至少避免了1440万例新冠死亡病例。随着其防护效果得到验证,mRNA疫苗研发也被扩展至更多传染病方向,包括流感病毒、呼吸道合胞病毒(RSV)、艾滋病毒(HIV)、寨卡病毒、埃布斯坦-巴尔病毒以及结核杆菌等,相关临床试验正在进行中。
不过,新冠研究也暴露出mRNA疫苗的一些局限:不同人群诱导的免疫反应差异较大且持续时间有限;SARS-CoV-2持续变异并出现新变种,进一步加剧免疫逃逸压力,使疫苗需要定期更新。此外,mRNA疫苗还面临制造流程复杂、成本较高、脂质纳米颗粒中mRNA分子数量控制不足、依赖冷链储存以及潜在非靶向效应等问题。
在此背景下,哈佛大学Wyss研究所、Dana-Farber癌症研究所(DFCI)及合作机构的多学科团队基于DNA折纸纳米技术开发了一种替代疫苗平台DoriVac。研究团队称,该平台兼具疫苗与佐剂功能,可在纳米尺度上对疫苗成分进行更精细的空间组织与呈递。
研究显示,DoriVac围绕多种病毒刺突蛋白中保守的肽段区域(HR2)进行设计,覆盖对象包括SARS-CoV-2、HIV和埃博拉等。在小鼠实验中,以SARS-CoV-2 HR2疫苗为例,DoriVac诱导了较强的抗原特异性抗体介导(体液)免疫反应以及T细胞介导(细胞)免疫反应。
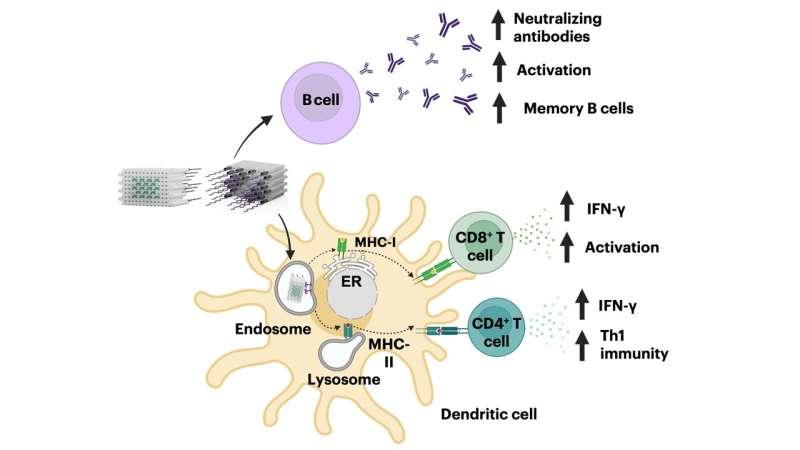
为评估其与人类免疫反应的相关性,团队进一步在Wyss研究所微流控人类器官芯片技术构建的前瞻性体外人类淋巴结模型(human LN Chip)中进行测试。结果显示,SARS-CoV-2 HR2 DoriVac疫苗可激活人类树突状细胞并显著提升炎症细胞因子分泌,同时增加多功能CD4+与CD8+ T细胞数量。
研究还将携带相同刺突蛋白变体的DoriVac疫苗与脂质纳米颗粒(LNP)包裹的SARS-CoV-2 mRNA疫苗进行对比。团队报告称,DoriVac在激活人类免疫反应方面与mRNA-LNP疫苗表现相当,同时具备更高稳定性,并被认为更易储存与制造。相关成果发表于《自然生物医学工程》。
共同通讯作者、Wyss研究所核心成员William Shih表示,DoriVac平台的优势之一在于对疫苗成分具备更高水平的控制能力,并可在分子层面针对特定免疫细胞进行“编程式”的免疫识别设计,以获得更理想的免疫反应。
据介绍,DoriVac由自折叠组装形成的方块状DNA纳米结构构成:一面以优化的纳米间距排列免疫增强佐剂分子,另一面展示所选抗原,包括肿瘤或病原体来源的肽段与蛋白质。项目负责人、共同作者杨(Claire)曾博士此前在肿瘤模型中展示了该平台通过纳米级精度呈递佐剂分子所带来的免疫增强效果。
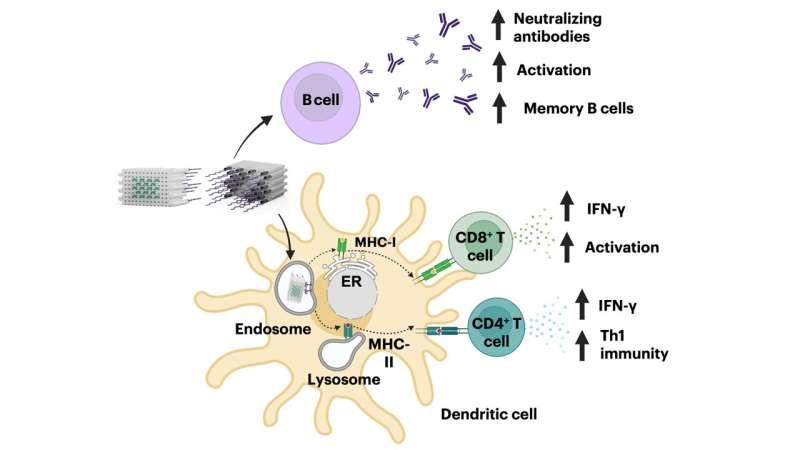
在传染病方向的研究中,曾博士与Shih团队前研究生Olivia Young博士等人合作,并与Wyss研究所Donald Ingber团队共同推进。研究团队在小鼠中观察到,与不含折纸结构的抗原与佐剂组合相比,DoriVac可引发更显著且更广泛的体液与细胞免疫激活,涉及多类关键免疫细胞。研究人员提到,产生抗体的B细胞数量、活化的抗原呈递树突状细胞,以及与长期保护相关的抗原特异性记忆与细胞毒性T细胞类型均有所增加,尤其在SARS-CoV-2 HR2疫苗组更为明显。
此外,团队还在小鼠中将针对完整SARS-CoV-2刺突蛋白的DoriVac疫苗与Moderna及辉瑞/BioNTech的mRNA-LNP疫苗进行正面比较,并采用通用的加强针方案。研究人员报告称,两者在抗病毒T细胞反应及产生抗体的B细胞反应方面表现相当。
研究团队指出,DoriVac不依赖mRNA-LNP疫苗所需的冷链储存,因而在资源匮乏地区的分发效率可能更高;同时也有望降低LNP配方疫苗制造的复杂性。另据DoriNano近期研究,DoriVac显示出良好的安全性表现。











