心脏病发作后,心脏往往难以恢复并维持能量供给,约三分之一患者随后进展为心力衰竭。心力衰竭在美国影响约680万人,且终生风险较高,预计美国每四位成年人中就有一人可能在一生中罹患该病。如何获得更持久的治疗手段,仍是医学研究的重要方向。
聚焦“能量危机”与线粒体
研究人员指出,心力衰竭在一定程度上可被视为心脏的“能量危机”。线粒体作为多数细胞内负责产生能量的细胞器,被认为可能在心脏功能恢复过程中发挥关键作用。
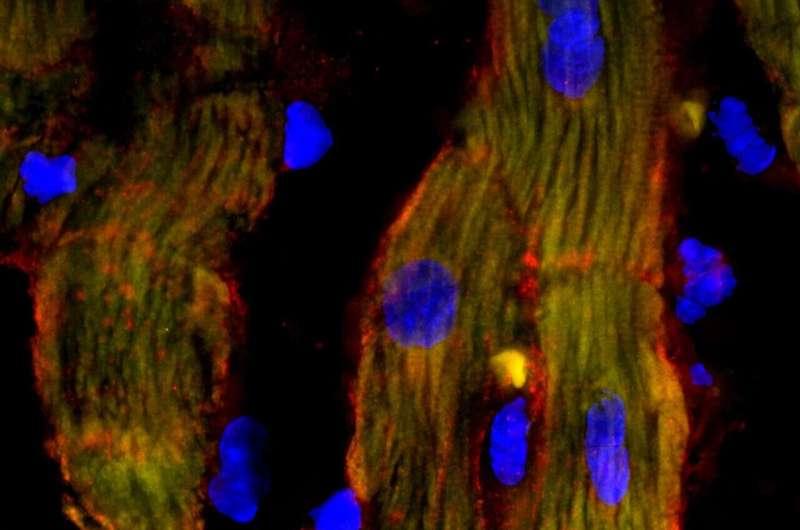
赖斯大学与贝勒医学院的研究团队近日报告称,他们利用一种基于CRISPR的技术,诱导心脏细胞将线粒体生成提升至更合适水平,从而为心力衰竭潜在疗法提供新路径。相关研究发表在《分子治疗》(Molecular Therapy)期刊。
该研究第一作者、赖斯大学生物工程助理研究教授马里奥·埃斯科巴尔表示,既往研究显示,激活特定基因可增加线粒体数量与功能,但传统策略可能使细胞“过度运转”,进而引发功能失调。研究团队提出的新方法旨在通过控制细胞内部调控通路,让细胞在不过度消耗的情况下更安全地制造更多线粒体。
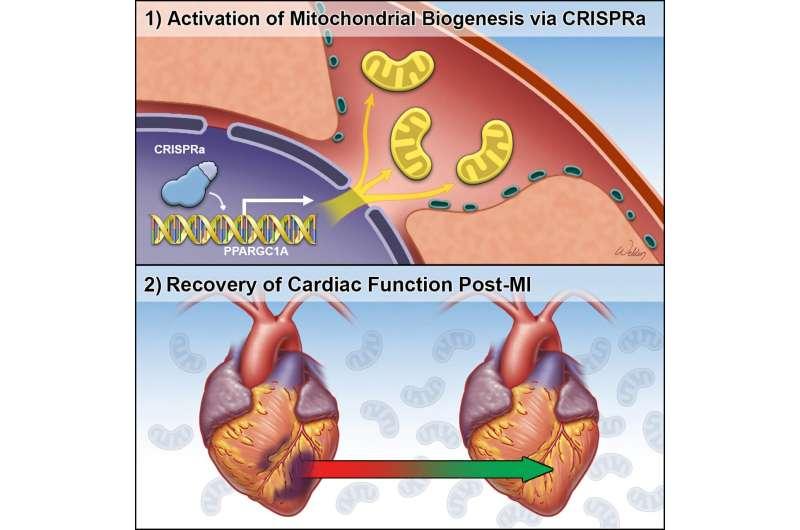
非编辑型CRISPR用于精细调控
CRISPR是一项可针对特定基因进行操作的技术,已推动多类疾病研究取得进展。此次研究中,团队开发的是一种“非编辑型”CRISPR系统,重点在于调控基因表达而非直接改写基因序列,并将其作为“开启”开关,促使细胞组装更多线粒体。
赖斯大学生物工程副教授、通讯作者艾萨克·希尔顿表示,该方法的特点在于调控的精细程度。研究并非强迫细胞过度表达某个基因,而是借助CRISPR以适度方式推动并微调细胞的自然调控系统,以在提升线粒体性能的同时维持细胞内平衡,这被认为是实现安全临床转化的重要要求。
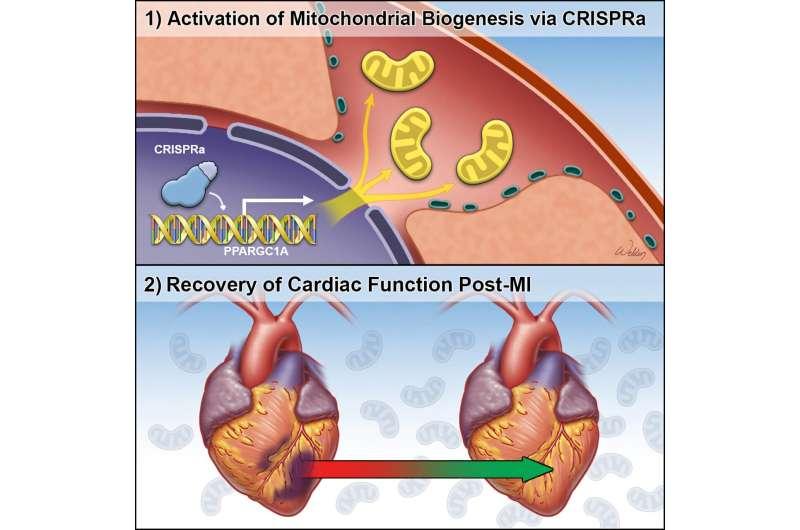
细胞、动物模型与人类心脏组织中的早期观察
研究团队在多种人类细胞类型中测试该系统时,观察到调控蛋白产生增加,线粒体功能与细胞能量水平随之增强。应用于负责心脏收缩的心肌细胞后,系统改善了其耗氧速率,提示线粒体功能得到提升。
此外,研究人员在动物模型以及来自正常与病变成人类心脏捐献组织中进行测试时,也观察到类似的线粒体功能改善。
埃斯科巴尔表示,这些结果为未来心力衰竭及其他代谢疾病治疗的研发提供了积极信号。
贝勒医学院外科教授、共同通讯作者拉维·甘塔指出,目前心力衰竭治疗多集中于降低心脏能量需求,以匹配受损的能量供给;传统方法随着时间推移可能引发额外并发症,因为未能解决根本问题。他表示,在心力衰竭患病率预计上升的背景下,开发更有效治疗手段尤为关键,而这项研究是向该方向迈出的重要一步。











